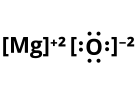Неорганическая химия
Неоргани́ческая хи́мия — наука, изучающая химические элементы и вещества ими образуемые кроме органических веществ. Является важной областью химии. Современная неорганическая химия изучет строение, свойства, химические превращения, реакционную способность, получение, генетические связи между неорганическими веществами, взаимосвязь между строением и свойствами веществ. Занимается разработкой методов очистки веществ и методами их синтеза. Основой теоретических знаний неорганической химии является периодический закон и Периодическая система химических элементов Дмитрия Ивановича Менделеева[1].
История развития
История неорганической химии развивалась одновременно с историей химии, естествознания и цивилизации. Первые химические открытия были сделаны около 3–5 тысяч лет до нашей эры, когда люди научились плавить медь, железо, бронзу и изготавливать стекло. В XVII веке были были открыты и исследованы многие простые газообразные вещества и соединения: азот, водород, кислород, хлор, диоксид углерода, оксиды азота и серы, другие газы. Роберт Бойль в своём труде «Химик-скептик» дал определение химическим элементам как веществам, которые не разлагаются на другие. Готфрид Эренфрид фон Шталь выдвинул теорию флогистона — особого вещества, которое выделяется при горении. Эта теория впоследствии была признана ошибочной, но помогла сформировать представления о сущности химических процессов[1].
В конце XVII века началось обособление знаний о неорганических веществах в отдельную область химии. Этот период часто связывают с именем Никола Лемери. М. В. Ломоносов и Антуан-Лоран де Лавуазье независимо друг от друга сформулировали закон сохранения массы для химических реакций. В XIX веке развитие неорганической химии было связано с внедрением атомной гипотезы и формированием атомно-молекулярной теории. К концу 1860-х годов было известно 63 химических элемента, классификацию которых основывали на периодическом законе, открытым Д. И. Менделеевым в 1869 году. В конце XIX — начале XX веков основное внимание в неорганической химии уделялось изучению состава и строения химических соединений. Во втором десятилетии XX века появились понятия об ионных и ковалентных химических связях, электроотрицательности, начали формироваться новые теории кислот и оснований. В середине XX века началось активное развитие производства химических источников тока, в частности литий-ионных аккумуляторов, суперконденсаторов и топливных элементов[1].
Структура науки
Существуют следующие разделы неорганической химии[1]:
- теоретическая;
- синтетическая;
- прикладная.
В соответствии с изучаемыми объектами неорганическая химия делится на:
- химию отдельных химических элементов;
- химию групп химических элементов, входящих в периодическую систему;
- химию исторически сложившихся групп химических элементов;
- химию групп химических элементов с родственным электронным строением;
- химию групп химических элементов и соединений с близкими составом, строением, свойствами или областями применения;
- химию соединений с определённым типом химической связи[1].
Методы синтеза
Для получения неорганических веществ используются методы, основанные на способности к взаимодействию простых веществ и неорганических соединений, на их физических и химических характеристиках. Синтез включает стадии: смешивание компонентов, активацию смеси, непосредственно химическую реакцию, выделение целевого продукта и его очистку[1].
Методы анализа
В неорганической химии для анализа неорганических веществ применяется препаративный метод (химический) и метод физико-химического анализа. Препаративный метод применяется с древних времен. Он включает в себя проведение реакций между исходными веществами и разделение полученных продуктов с использованием процессов перегонки, возгонки, кристаллизации, фильтрации и других[1].
Метод физико-химического анализа был разработан Н. С. Курнаковым и его последователями. Этот метод основан на измерении различных физических свойств систем, содержащих два, три и более компонента. Полученные данные представляются в виде диаграмм. Их анализ позволяет определить состав и природу продуктов, образующихся в системе, без необходимости их выделения для дальнейшего анализа. Физико-химический анализ помогает определить пути синтеза веществ и предоставляет научную основу для процессов переработки руд, получения солей, металлов, сплавов и других важных промышленных материалов[1].
Классификация химических элементов
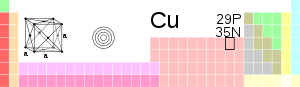
Классификация химических элементов в неорганической химии представлена в Периодической системе химических элементов Д. И. Менделеева, представляющая собой графическое выражение Периодического закона. Все открытые химические элементы располагаются в Периодической системе в соответсствии с возрастанием их атомных масс (во времена Д. И. Менделеева эту величину называли атомным весом). Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от величины зарядов ядер их атомов[2].
Простые вещества
Химические вещества, состоящие из одного вида атомов, отличаются от сложных веществ. Простые вещества могут быть металлами или неметаллами, в зависимости от типа их химической связи[3].
Металлы
Все металлы, за исключением ртути (Pb), находятся в твёрдом состоянии и обладают схожими свойствами. Металлы — вещества, обладающие ковкостью, пластичностью и тягучестью, они имеют металлический блеск, хорошо проводят тепло и электричество. Среди них есть как мягкие (например, щелочные металлы (литий (Li))), так и твёрдые (например, хром (Cr) и титан (Ti))[4].
Неметаллы
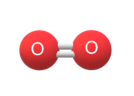
Неметаллы — химические элементы, которые образуют простые вещества без физических свойств металлов. Они могут находиться в различных состояниях: быть газами (гелий, водород, кислород, азот, хлор), жидкостями (бром) или твёрдыми веществами (сера, углерод, кристаллический йод)[4].
Сложные вещества
Сложные неорганические вещества делят на оксиды, кислоты, основания, соли.
Оксиды
Сложные вещества состоят из двух химических элементов, один из которых — кислород в степени окисления -2.
Оксиды — класс неорганических соединений, которые широко распространены в природе. Примером такого соединения может служить кварц SiO2. Оксиды также содержатся в большинстве руд чёрных металлов, например, в красном железняке Fe2O3 и магнитном железняке Fe3O4[4].
Оксиды бывают трех типов: твёрдые, жидкие и газообразные.
Солеобразующие оксиды делятся на три группы: основные, кислотные и амфотерные.
Основные оксиды имеют степень окисления I—II; кислотные — V—VII; амфотерные — III—IV (за исключением оксида цинка ZnO, оксида бериллия BeO, оксида олова (II) SnO, оксида свинца (II) PbO)[5].
Кислоты
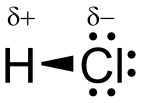
Кислоты — сложные вещества, молекулы которых содержат атомы водорода, способные замещаться на металл, и кислотный остаток (например, соляная кислота HCl)[4].
Существует несколько способов классификации кислот:
- по содержанию кислорода (бескислородные и кислородсодержащие);
- по количеству атомов водорода (одноосновные, двухосновные, трехосновные, многоосновные);
- по силе (сильные и слабые);
- по устойчивости (устойчивые и неустойчивые);
- по летучести (летучие, нелетучие);
- по растворимости в воде (растворимые и нерастворимые)[6].
Основания
Основания — сложные вещества, состоящие из ионов металлов и связанных с ними гидроксид-ионов. Они могут быть как бинарными соединениями (например, вода H2O), так и сложными веществами, в состав которых входят металл, кислород и водород (например, гидроксид калия KOH). Названия оснований образуются путем добавления слова «гидроксид» к названию металла в родительном падеже.
Основания делятся на две группы по отношению к воде:
- растворимые — называются щелочами (например, гидроксид натрия (NaOH), гидроксид кальция Ca(OH)2, гидроксид калия KOH, гидроксид бария Ba(OH)2;
- нерастворимые — гидроксид меди (II) Cu(OH)2, гидроксид железа (II) Fe(OH)2)[4].
Соли
Соли — сложные вещества, состоящие из ионов металлов и кислотных остатков (например, сульфат кальция CaSO4), которые получаются при замещении атомов водорода в кислоте на ионы металла. Названия солей формируются из двух слов: название иона, образованного кислотным остатком, в именительном падеже и название иона металла — в родительном.
Соли по растворимости в воде делят на:
- растворимые;
- нерастворимые;
- малорастворимые.
Растворимость солей определяют по таблице «Растворимость оснований, кислот и солей в воде»[4].
Существуют различные типы солей[2][7]:
- кислые соли (продукты неполного замещения атомов водорода в кислоте на металл), например, гидросульфат калия KHSO4;
- основные соли (продукты неполного замещения гидроксогрупп в основании на кислотный остаток), например, гидроксохлорид магния Mg(OH)Cl ;
- средние соли (все атомы водорода в молекулах кислоты замещены на атомы металла), например, сульфат калия K2SO4;
- двойные соли (в их состав входит комплексный катион или комплексный анион), например, гексацианоферрат калия K4[Fe(CN)6] .
Литература
- Глинка Н. Л. Общая химия: учебное пособие для СПО. — М.: КноРус, 2019. — 360 c.
- Глинка Н. Л. Общая химия: учебное пособие для вузов / под ред. А. И. Ермакова. — М.: Интеграл-Пресс, 2003. — 728 с.
- Карапетьянц М. Х. Общая и неорганическая химия: учебник / под ред. М. Х. Карапетьянц, С. И. Дракин. — М.: Ленанд, 2018. — 600 c.
- Общая химия. Учебник / под ред. С. Ф. Дунаева. — М.: Academia, 2017. — 160 c.
- Общая и неорганическая химия: учебное пособие / под ред. В. В. Денисова, В. М. Таланова. — Рн/Д: Феникс, 2018. — 144 c.
Примечания
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 1,7 Неорганическая химия. Большая Российская энциклопедия. Дата обращения: 20 мая 2024.
- ↑ 2,0 2,1 Химия. Базовый уровень 11 класс. Учебник / под ред. О. С. Габриелян. — М.: Дрофа, 2014. — 221 с.
- ↑ Простые и сложные вещества. Skysmart. Дата обращения: 20 мая 2024.
- ↑ 4,0 4,1 4,2 4,3 4,4 4,5 Химия. 8 класс. Учебник / под ред. О. С. Габриелян. — М.: Дрофа, 2019. — 284 с.
- ↑ Оксиды. Фоксфорд. Дата обращения: 21 мая 2024.
- ↑ Классификация и номенклатура кислот. Фоксфорд. Дата обращения: 20 мая 2024.
- ↑ Классификация и номенклатура солей. Фоксфорд. Дата обращения: 20 мая 2024.
Данная статья имеет статус «готовой». Это не говорит о качестве статьи, однако в ней уже в достаточной степени раскрыта основная тема. Если вы хотите улучшить статью — правьте смело! |
Данная статья имеет статус «проверенной». Это говорит о том, что статья была проверена экспертом |