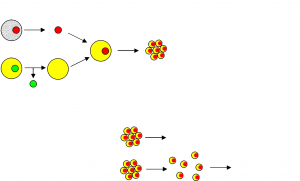
Клонирование

Клонирование (от др. греч. κλών «ветвь, побег, отпрыск») — получение как бесполым естественным путём, включая вегетативное размножение, так и при помощи биотехнологических методов генетически тождественных (клонов) организмов, клеток или молекул[1]. Клон — организм, ДНК которого идентична ДНК другого организма. Использование методов клонирования позволяет значительно сократить сроки получения принципиально новых свойств у селекционных сортов сельскохозяйственных растений и пород животных, штаммов микроорганизмов. Биоинженерия дает шанс человеку излечения от десятков болезней, считающихся до сих пор неизлечимыми, включая рак и старение организма, открывает новые горизонты в области регенеративной биомедицины — клонирование органов и тканей человека[2].
История термина
Термин «клон» происходит от греческого слова «klon», что означает — веточка, побег, черенок, и имеет отношение, прежде всего к вегетативному размножению. Позже клоном стали называть не только всю такую группу, но и каждое отдельное растение в ней (кроме первого), а получение таких потомков — клонированием. Клонирование растений черенками, почками или клубнями в сельском хозяйстве, в частности в садоводстве, известно уже более четырех тысяч лет[3].
Типы клонирования
Существует четыре типа клонирования:
- естественное клонирование;
- молекулярное клонирование;
- репродуктивное клонирование;
- терапевтическое клонирование.
Клонирование гена производит копии генов. Это самый распространенный и обычный тип клонирования произведённого исследователями в Национальном Научно-исследовательском институте Генов Человека (ННГЧ)[2].
Естественное клонирование
Естественное клонирование — это получение клонов без использования методов генной инженерии[4]. Это может произойти случайно в случае идентичных близнецов, которые образуются, когда оплодотворённая яйцеклетка расщепляется, создавая два или более эмбрионов, несущих почти идентичную ДНК. Оно также может быть частью бесполого размножения, представляющего собой процесс, при котором один родительский организм сам по себе производит генетически идентичное потомство[5].
Молекулярное клонирование
Молекулярное, включающее генетическое клонирование, представляет собой технологическое создание (клонирование) необходимого количества генетического материала (фрагментов генов, генов, молекул ДНК) с помощью живых организмов. Для этого, обычно изменённую, полинуклеотидную последовательность встраивают в геном бактериофага или плазмиду (вектор) и привносят в клетки прокариотов или эукариотов, которые затем выращивают в питательной среде в лабораторных условиях (in vitro). Размножаясь, эти клетки обеспечивают сохранение данного вектора и клонируют необходимую вставку последовательности нуклеотидов, в точности сохраняя её структуру. Получаемые таким способом гибридные молекулы называются рекомбинантными. Метод молекулярного клонирования применяется для исследования биологических молекул и создания рекомбинантных биологических структур с заданными параметрами, клонирования тканей и других научных и производственных целей[6].
Репродуктивное клонирование
Это искусственное воспроизведение в лабораторных условиях генетически точной копии любого живого существа. Такой тип клонирования помогает восстановить исчезнувшие организмы или сохранить их популяцию[7].
Терапевтическое клонирование
Главная цель терапевтического клонирования — получение культуры стволовых клеток, генетически идентичных клеткам донора, для разработки новых методик и терапии различных заболеваний[8]. В терапевтическом клонировании используется процесс, известный как пересадка ядер соматических клеток, (замена ядра клетки, исследовательское клонирование и клонирование эмбриона), состоящий в изъятии яйцеклетки (ооцита) из которой было удалено ядро, и замена этого ядра ДНК другого организма. После многих митотических делений культуры (митозов культуры), данная клетка образует бластоцисту (раннюю стадию эмбриона состоящую из приблизительно 100 клеток) с ДНК почти идентичным первичному организму.
Методы клонирования
Методы трансплантации ядер
В нашей стране Конюховым Б. В. и Платоновым Е. С. в 1985 году был разработан метод менее травматического переноса ядер методом микроманипуляции. Он протекает в два этапа: сначала тонкой микропипеткой прокалывают зоны пеллюцида и плазматической мембраны и извлекают пронуклеусы, а затем другой пипеткой, большего диаметра (12 мкм) в то же отверстие вводят диплоидное ядро донора. В этом случае меньше травмируется цитоплазма зиготы и транспортируемое ядро донора[9].
Трансплантация ядер может осуществляться и другим способом, с использованием цитохалазинов (веществ, синтезируемых грибами).
Цитохалазин-В разрушает структуру микрофиламентов и способствует уникальному расположению ядра. Ядро остается соединённым с клеткой тоненьким стебельком цитоплазмы. При центрифугировании этот мостик разрывается, образуются безъядерные клетки (цитопласты) и кариопласты, представляющие собой ядра, окружённые тонким слоем цитоплазмы и цитоплазматической мембраной. Цитопласты отделяют от интактных клеток в градиенте плотности. Они сохраняют способность прикрепляться к поверхности культурального сосуда и могут быть использованы для слияния с кариопластами других клеток с целью получения жизнеспособной клетки.
SLIC (Sequence and Ligation-Independent Cloning) метод клонирования
Стив Элледж и Мами Ли разработали оригинальный методом клонирования. Новый метод получил название SLIC (Sequence and Ligation-Independent Cloning). Новинка является модификацией известного метода LIC (Ligation-Independent Cloning) — клонирования без использования лигазы. Для того чтобы вставить фрагмент ДНК в вектор при помощи классического метода LIC, достаточно смешать вектор и вставку, на концах которых расположены протяженные одноцепочечные участки, комплементарные друг другу. При этом вставка «прилипает» к вектору, образуя рекомбинантную плазмиду с никами в обеих цепях. Полученной плазмидой трансформируют Е.coli, система репарации которой восстанавливает нормальную структуру плазмиды[10].
Метод SLIC — это то же самое, что и LIC с единственной разницей: «слипание» вектора и вставки проводят в присутствии белка RecA. Эта незначительная модификация метода позволяет добиться достаточно высокого выхода (1 нг. вектора способен дать 3900 трансформантов) а также упростить саму процедуру клонирования. Так если для классического метода LIC необходимо точно подогнать размер одноцепочечных участков у вектора и вставки (чтобы в итоге на стыке вектора и вставки получились ники), то метод SLIC допускает наличие протяженных гэпов.
Фактор RecA — один из ключевых факторов репарации и рекомбинации E.coli. Связываясь с одноцепочечным участком ДНК, RecA стимулирует процесс «strand exchange» (в ходе этого процесса одноцепочечный участок одной молекулы ДНК встраивается в гомологичный двухцепоченый участок другой молекулы ДНК, образуя D-петлю). Очевидно, добавление RecA in vitro на шаге клонирования позволяет E.coli эффективнее репарировать плазмиду in vivo.
Для успешного клонирования необходимо наличие 30-ти нуклеотидных участков гомологии по краям вектора и вставки. Получать одноцепочечные участки предлагается с помощью T4 ДНК-полимеразы без добавления нуклеотидов. При помощи SLIC в один вектор можно запихнуть сразу 5 вставок в одну стадию без снижения выхода. Наконец, высокий выход позволяет использовать метод SLIC при клонировании библиотек[11].
Метод генетического перепрограммирования клеток кожи
Этот метод менее трудоёмкий, чем тот, что использовался при клонировании овцы Долли. В связи с этим возникли опасения, что однажды он будет использован для обработки эмбрионов человека, дабы формировать детей «по заказу».
Учёные, благодаря этому методу получившие мышат из клеток кожи взрослых особей, обнаружили: такая технология намного более эффективна, чем способ создания Долли, а побочных эффектов у неё меньше — следовательно, она лучше подходит для использования применительно к человеку.
Для клонирования мышей ученые вводили клетки кожи, взятые у взрослой особи, в ткани эмбриона на ранней стадии развития, полученного путём экстракорпорального оплодотворения (ЭКО). Некоторые из детёнышей оказались частичными клонами особей-доноров, а некоторые, как и Долли, стопроцентными[12].
Однако, в отличие от «метода имени Долли», этот способ настолько прост и эффективен, что возникли опасения: в клиниках, где практикуется ЭКО человека, им могут воспользоваться для помощи бесплодным супружеским парам, которые мечтают о полностью «своём» в биологическом отношении ребёнке.
Метод предполагает генетическое перепрограммирование клеток кожи, в результате которого они возвращаются в квазиэмбриональное состояние. В прошлом году, когда эта революционная методика впервые была применена к клеткам кожи человека, Католическая церковь и президент Джордж Буш высоко оценили её как нравственно-приемлемый способ получения эмбриональных стволовых клеток, не сопряженный с необходимостью создавать или уничтожать человеческие эмбрионы.
Однако тот же метод уже используется в иных целях — для воспроизводства потомства лабораторных мышей, которое является либо стопроцентными клонами, либо генетическими «химерами» взрослых мышей, клетки кожи которых подверглись перепрограммированию.
Эксперименты на мышах показали, что в принципе теперь возможно взять клетку кожи человека, перепрограммировать её для возврата в эмбриональное состояние, а затем ввести её в эмбрион человека на ранней стадии. В результате получится ребёнок, обладающий некоторыми общими генами не только с родителями эмбриона, но и с человеком, у которого были взяты клетки кожи.
Такой ребёнок является химерой — генетической «помесью» двух или большего числа особей — так как некоторые из его клеток происходят от эмбриона, а другие — от клетки кожи. Фактически у такого ребёнка будет три биологических родителя. Известны химеры человека, возникающие в естественных условиях — когда в матке соединяются два эмбриона. Часто подобные люди являются совершенно нормальными и здоровыми. По словам доктора Ланцы, нет причин предполагать, что люди-химеры, созданные при помощи нового метода, будут нездоровы.
Более того, эксперименты на мышах показали, что возможно создавать полные клоны — детенышей, которые на 100 % идентичны взрослой особи в генетическом плане. Этого удалось достигнуть, используя разновидность дефективных эмбрионов мышей с четырьмя наборами хромосом вместо нормального числа — двух.
Этот «тетраплоидный» эмбрион, развиваясь, превращался исключительно в плаценту плода; когда же в него ввели перепрограммированную клетку кожи, остальная часть плода развилась из этой единственной клетки и сделалась стопроцентным клоном взрослой особи, кожа которой использовалась.
Никто из учёных, разрабатывающих методы перепрограммирования клеток для производства индуцированных плюрипотентных стволовых клеток (induced Puripotent Stem, сокращенно iPS) — так называют эмбриональные клетки — не планирует применять их в репродуктивной медицине человека. Главная цель учёных — наладить производство стволовых клеток для терапевтического лечения таких заболеваний, как болезнь Паркинсона, болезнь Альцгеймера и инсульт[13].
Виды клонирования
Наибольшее внимание учёных и общественности привлекает клонирование многоклеточных организмов, которое стало возможным благодаря успехам генной инженерии. Создавая особые условия и вмешиваясь в структуру ядра клетки, специалисты заставляют её развиваться в нужную ткань или даже в целый организм. Допускается принципиальная возможность воспроизведения даже умершего организма, при условии сохранения его генетического материала.
Различают полное (репродуктивное) и частичное клонирование организмов. При полном воссоздаётся весь организм целиком, при частичном — организм воссоздаётся не полностью (например, лишь те или иные его ткани или органы).
Репродуктивное клонирование кроме научных целей может применяться для восстановления исчезнувших видов или сохранения редких видов.
Одно из перспективных применений клонирования тканей — клеточная терапия в медицине. Такие ткани, полученные из стволовых клеток пациента, могли бы компенсировать недостаток и дефекты собственных тканей организма и не отторгаться при трансплантации. Это так называемое терапевтическое клонирование. Терапевтическое клонирование предполагает, что в результате намеренно не получается целый организм. Его развитие останавливают заранее, а получившиеся эмбриональные стволовые клетки используют для получения нужных тканей или других биологических продуктов. Эксперименты показывают, что терапевтическое клонирование может быть с успехом применено для лечения некоторых заболеваний, считавшихся неизлечимыми[14].
Клонирование растений

Биотехнология, а в частности клеточная биология, как наука получила обширное развитие в XX—XXI веке. На фоне активного развития клеточных технологий, и острой потребности в БАВ, особый интерес начали уделять технологии in vitro. В частности, микроклональное размножение растений дает возможность выращивать древесные растения достаточно быстро и независимо от погодных и климатических условий. В отличие от семенного размножения, при котором потомки не обладают всеми лучшими качествами материнского растения, растения-регенеранты являются точной копией (клоном) исходника. Это даёт преимущество для сохранения необходимых свойств у регенеранта. Например, это весьма актуально для редких и трудноразмножаемых растений, как Секвойяде́ндрон гига́нтский (лат. Sequoiadendron giganteum)
Так же благодаря технологии культур клеток in vitro можно культивировать редкие растения и эндемики с целью получения вторичных метаболитов для нужд фармацевтической промышленности. Данная технология успешно реализуется в разных странах (Германия, Южная Корея, Япония, Нидерланды, Россия). При этом получаемое сырье экологически чисто, и производство не привязано географически. Актуальность этого направления особо высока для получения соединений, которые невозможно получить химическим путём или выделить из растений природных популяций.
Клонирование животных
Идея клонирования животных зародилась в учёных кругах более ста лет назад. Первыми клонированными животными являются представители класса амфибий. Английский эмбриолог Джордж Гёрдон проводил эксперименты по созданию копий лягушек. В данных опытах производилось пересадка ядер кишечника головастиков. В результате эксперимента было доказано, что первичные половые клетки могут сохраниться с пересаженными в них ядрами. Данное исследование встретило колоссальную негативную реакцию со стороны общественности, и работы по проведению клонирования амфибий были прекращены на несколько лет. Позже в начале 1970-х годов была произведена пересадка ядер из соматической клетки взрослой лягушки в ооциты, из которых позже выросли головастики, а затем и взрослые лягушки[15].
После успешного клонирования лягушек учёные принялись проводить эксперименты по созданию копий представителей класса млекопитающих. Ходят слухи, что в закрытых лабораториях советским учёным в конце восьмидесятых годов удалось получить несколько клонов домовой мыши. Официально первым млекопитающим, которое было получено путем пересадки ядра из соматической клетки в генеративную, является овца по кличке Долли. Клонирование Долли произошло в результате деятельности шотландской группы исследователей в 1996 году. С тех пор были получены клоны целого ряда млекопитающих[16].
Список клонированных животных
- 1970 год — успешное клонирование лягушки.
- 1985 год — клонирование костных рыб.
- 1986 год — первое клонирование мыши из эмбриональных клеток.
- 1996 год — клонирование овцы Долли от клеток взрослого животного[17].
- 1998 год — первое клонирование коровы[18].
- 1999 год — первое клонирование козла.
- 2001 год — первое клонирование кошки.
- 2002 год — первое клонирование кролика.
- 2003 год — первое клонирование быка, мула, оленя.
- 2004 год — первый опыт клонирования кошек с коммерческими целями.
- 2005 год — первое клонирование собаки[19].
- 2006 год — первое клонирование хорька.
- 2007 год — второе клонирование собаки.
- 2008 год — третье клонирование собаки (лабрадора по кличке Чейс, по государственному заказу). Начало коммерческого клонирования собак.
- 2009 год — первое успешное клонирование верблюда (по кличке Инджаз). Также впервые на Ближнем Востоке (а именно в Иране) была успешно клонирована коза (предыдущие страны, которым это удалось: США, Великобритания, Канада, Китай).
- 2011 год — клонирование восьми щенков койота.
- 2018 год — клонирование двух обезьян — макак-крабоедов.
- 2019 год — клонирование британского короткошерстного кота.
- 2022 год — первое клонирование лошади.
Клонирование для воссоздания вымерших животных
Клонирование используется для воссоздания естественных популяций вымерших животных.
Клонирование испанского козерога
Впервые путем клонирования было воскрешено вымершее животное, хотя клон умер через несколько минут после рождения.
Результаты, опубликованные 23 января в журнале Theriogenology, описывают использование замороженной кожи в 2003 году для клонирования букардо, или пиренейского козерога, подвида испанского козерога, который вымер в 2000 году.
Данный подвид пиренейских козлов полностью исчез к 2000 году (причины вымирания точно не известны). Последний представитель вида, самка по имени Селия (Celia), погибла в 2000 году. Но до того (в 1999 году) Хосе Фольк (Jose Folch) из Исследовательского центра сельского хозяйства и технологий Арагона (CITA) взял у Селии несколько клеток кожи с целью анализа и сохранения в жидком азоте. Этот генетический материал был использован в первой попытке клонировать вымерший подвид[20].
Экспериментаторы переносили ДНК букардо в яйцеклетки домашней козы, лишённые собственного генетического материала. Полученные эмбрионы подсаживали суррогатным матерям — самкам других подвидов испанского козла или гибридных видов, полученных скрещиванием домашних и диких коз. Таким образом было создано 439 эмбрионов, 57 из которых были имплантированы в суррогатные матки. Всего семь операций закончилось беременностью и только одна коза, в конце концов, родила самку букардо, умершую спустя семь минут после рождения от проблем с дыхательной системой.
Клонирование мамонтов
Лаборатория Джорджа Черча (George Church) из Гарвардского университета (США) в середине октября 2014 года объявила о начале проекта по «воскрешению» мамонтов. Шансы на воскрешение мамонтов появились благодаря появлению в 2012 году революционной технологии «перезаписи» генома CRISPR/CAS, которая позволяет точечным образом менять и удалять произвольные гены в ДНК млекопитающих. Используя эту методику, Черч и его коллеги смогли успешно вставить в геном клеток кожи слона гены, предположительно отвечающие за типичные признаки мамонта — маленькие уши, толстый слой подкожного жира, длинную шерсть и бурый цвет. Клетки пережили эту трансформацию и сейчас учёные думают над тем, как их можно превратить в настоящую кожную ткань[21].
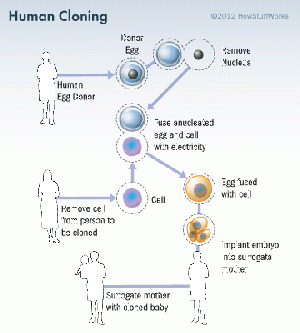
Клонирование человека
Клонирование человека — это создание эмбриона и дальнейшее выращивание из эмбриона человека, имеющего генотип ныне существовавшего индивида.
Клонирование человека, как правило, осуждается из-за психологических, социальных и физиологических рисков[22]. Так как клонированный эмбрион подсаживается в матку, то перед переносом требуется тщательное молекулярное исследование эмбриона, чтобы убедиться в его здоровье. При этом клонировать человека как личность нельзя. Можно создать копию с таким же генотипом, но не фенотипом — всех характеристик организма, в том числе внешних. Кроме того, есть множество технических препятствий и для клонирования генотипа. Ещё никогда у ученых не получалось клонировать млекопитающих со 100 % результативностью, а большинство беременностей заканчивается выкидышем[23].
Законодательство о клонировании человека
Во многих государствах использование такой технологии применительно к человеку официально — запрещено: Россия, Германия, Франция, Испания, Италия, США, Япония, Бельгия, Нидерланды, Швеция и другие.
8 марта 2005 год. Генеральная ассамблея ООН большинством голосов приняла декларацию о всеобщем запрете клонирования человека[24]. Из представителей 191 страны «за» проголосовали 84, «против» — 34, воздержались — 37.
Клонирование человека в России
Россия не осталась в стороне и приняла Федеральный закон «О временном запрете на клонирование человека» от 20 мая 2002 год № 54-ФЗ[25].
Закон вводил запрет на клонирование человека, исходя из принципов уважения человека, признания ценности личности, необходимости защиты прав и свобод человека и учитывая недостаточно изученные биологические и социальные последствия клонирования человека. С учётом перспективы использования имеющихся и разрабатываемых технологий клонирования организмов, предусматривается возможность продления запрета на клонирование человека или его отмены по мере накопления научных знаний в данной области, определения моральных, социальных и этических норм при использовании технологий клонирования человека.
Согласно ст. 1 Закона, временный запрет вводился на пять лет, который истёк в июне 2007 года, и в последующие два года вопрос клонирования человека никак не регулировался российским законодательством. Однако в конце марта 2010 года запрет на клонирование человека в России был продлён путём принятия в ст. 1 Закона поправки, продлевающую запрет на клонирование человека на неопределённый срок — до вступления в силу закона, устанавливающего порядок применения биотехнологий в этой области.
Причина запрета указывается в пояснительной записке к законопроекту: «Клонирование человека встречается с множеством юридических, этических и религиозных проблем, которые на сегодняшний день ещё не имеют очевидного разрешения».
Примечания
- ↑ Клонирование в биологии (неопр.). Дата обращения: 24 июля 2023.
- ↑ 2,0 2,1 И.А. Миненко, Д.Г. Сердюков. К вопросу об истории клонирования // Вестник новых медицинских технологий : журнал. — 2014. — № 1. — С. 1—9.
- ↑ История экспериментов с клонированием. РИА новости (05.07.2021). Дата обращения: 17 июля 2023.
- ↑ Естественное клонирование (Natural Cloning) (англ.). Дата обращения: 5 июня 2023.
- ↑ Информационный бюллетень по клонированию (Cloning Fact Sheet) (англ.). Дата обращения: 24 июля 2023.
- ↑ Молекулярное клонирование, или как засунуть в клетку чужеродный генетический материал. Биомолекула (30.10.2011). Дата обращения: 22 июля 2023.
- ↑ Репродуктивное клонирование. Рамблер/новости (23.11.2023). Дата обращения: 18 июля 2023.
- ↑ Терапевтическое клонирование. Studfiles (30.08.2022). Дата обращения: 5 июля 2023.
- ↑ Методы трансплантации ядер. StudFiles. Дата обращения: 17 июля 2023.
- ↑ SLIK ((sequence and ligation-independent cloning). Studizba. Дата обращения: 16 июля 2023.
- ↑ В.Ю. Ушаков. SOS-система репарация ДНК у бактерий // Вестник Пермского университета : журнал. — 2010. — № 2. — С. 1—12.
- ↑ Метод генетического перепрограмирования клеток кожи. Яндекс.учебник. Дата обращения: 22 июля 2023.
- ↑ Кайгородцев М.А. Клонирование человека и отношению общества к новому методу. Студенческий научный форум. Дата обращения: 15 июня 2023.
- ↑ Волков Олег. Использование клонирования в медицине. DTF (20.05.2019). Дата обращения: 20 июля 2023.
- ↑ Основы биотехнологии. Дата обращения: 15 июля 2023.
- ↑ Что такое клонирование?. Наука.Club. Дата обращения: 14 июля 2023.
- ↑ Клонирование млекопитающих в СССР. Дата обращения: 14 июля 2023.
- ↑ Японские ученые клонируют корову (англ.). BBS. Дата обращения: 22 июля 2023.
- ↑ Первое клонирование собаки (англ.). Дата обращения: 22 июля 2023.
- ↑ Создан первый клон вымершего животного (англ.). National Geographic. Дата обращения: 24 июля 2023.
- ↑ Генетики успешно вставили гены мамонта в ДНК в клетках слонов (англ.). РИА новости. Дата обращения: 23 июля 2023.
- ↑ Легкоева М.В. Этические и научные проблемы клонирования // Молодой ученый : журнал. — 2021. — № 46. — С. 24—26.
- ↑ Клонирование человека. Дата обращения: 15 июля 2023.
- ↑ Разделенная ООН: запрет на клонирование человека (англ.). Дата обращения: 22 июля 2023.
- ↑ Федеральный Закон " О временном запрете на клонирования человека". Консультант Плюс. Дата обращения: 24 июля 2023.
Данная статья имеет статус «готовой». Это не говорит о качестве статьи, однако в ней уже в достаточной степени раскрыта основная тема. Если вы хотите улучшить статью — правьте смело! |
Данная статья имеет статус «проверенной». Это говорит о том, что статья была проверена экспертом |