Олеиновая кислота
| Олеиновая кислота | |
|---|---|
  | |
| Общие | |
| Систематическое наименование |
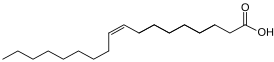
цис-9-октадеценовая кислота |
| Традиционные названия | олеиновая кислота |
| Рац. формула | C17H33COOH |
| Физические свойства | |
| Состояние | бесцветная жидкость |
| Молярная масса | 282,46 г/моль |
| Плотность | 0,895 (+18 °C, г/см³) |
| Динамическая вязкость | (в мПа·с): 25,6 (+30 °C) |
| Термические свойства | |
| Температура | |
| • плавления | +16,3 °C |
| • кипения | 360 °C; при 10 мм рт. ст.: 225—226 °C |
| Давление пара | 3 (175 °C); 10 (225 °C); 15 (232 °C); 100 (286 °C) в мм. рт. ст. |
| Химические свойства | |
| Растворимость | |
| • в воде | не растворима |
| • в бензоле | растворима |
| • в хлороформе | растворима |
| • в этаноле | смешивается |
| • в диэтиловом эфире | смешивается |
| Оптические свойства | |
| Показатель преломления | (для D-линии натрия): 1,4582 (+20 °C) |
| Классификация | |
| Рег. номер CAS | 112-80-1 |
| SMILES | |
| RTECS | RG2275000 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
| Олеиновая кислота | |
|---|---|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. |
Олеи́новая кислота́ (C18H34O2) — омега-9 жирная кислота, представляющая собой бесцветную или слегка желтоватую жидкость без запаха. Её температура плавления составляет 13—14 °C, а температура кипения — 360 °C. Кислотное число варьируется от 197 до 204 мг КОН/г. В промышленности её получают из смеси жирных кислот, образующихся при гидролизе жиров и растительных масел, в основном оливкового[1].
Олеиновая кислота используется в пищевой промышленности как эмульгатор и консервант, в косметике — для увлажнения кожи и волос, в фармацевтике — как основа для мазей и кремов, а также в химической промышленности для производства мыла и смазочных материалов. В текстильной и кожевенной отраслях она придаёт волокнам мягкость и эластичность[1].
История открытия
Олеиновая кислота является одной из наиболее распространённых жирных кислот в природе и входит в состав многих растительных масел, особенно оливкового, арахисового и пальмового. История её открытия тесно связана с развитием органической химии и изучением жиров в XVIII-XIX веках[2].
Ранние исследования жиров
Первые упоминания о веществах, связанных с олеиновой кислотой, встречаются в работах химиков XVIII века, изучавших состав жиров и масел. В 1779 году шведский химик Карл Вильгельм Шееле (швед. Carl Wilhelm Scheele) обнаружил, что при щелочном гидролизе жиров образуются мыло и глицерин. Хотя он не выделил отдельные жирные кислоты, его работа заложила основу для дальнейшего анализа состава жиров[2].
В начале XIX века химики начали разделять жиры на составляющие их кислоты. Во Франции Мишель Эжен Шеврёль (фр. Michel Eugène Chevreul) провёл систематические исследования жиров и в 1813—1823 годах опубликовал результаты своей работы в труде фр. «Recherches sur les corps gras d'origine animale» («Исследования о жирах животного происхождения»). Он впервые выделил и описал несколько жирных кислот, в том числе стеариновую и пальмитиновую, и ввёл термин «кислота» применительно к жирам. Мишель Шеврёль также описал вещество, которое он назвал «олеин» (от лат. oleum — масло), выделив его из оливкового масла. Он установил, что это вещество представляет собой кислоту, которая остаётся жидкой при комнатной температуре, в отличие от твёрдых стеариновой и пальмитиновой кислот[2].
Свойства вещества
Химическое строение
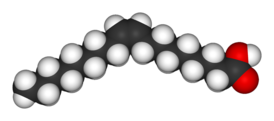
Цис-конфигурация олеиновой кислоты: молекула содержит цис-двойную связь между 9-м и 10-м атомами углерода, что создаёт угловое изгибание и препятствует плотной упаковке молекул, сохраняя жидкую форму при комнатной температуре (+13,4 °C).
Изомеризация: под воздействием катализаторов (например, диоксида азота) цис-изомер превращается в транс-изомер — элаидиновую кислоту, с линейной структурой и температурой плавления +44 °C. Эта реакция использовалась для анализа состава растительных масел[3].
Физические свойства
Данное вещество при комнатной температуре представляет собой прозрачную желтоватую жидкость, обладающую маслянистой текстурой. Оно характеризуется нейтральным запахом и нерастворимостью в воде, однако проявляет высокую растворимость в органических растворителях. Молекулярная масса соединения составляет 282,46 г/моль. Температура плавления находится на уровне 13,4 °C, а температура кипения достигает 360 °C. Плотность вещества составляет 0,895 г/см3[4].
Химические свойства
Транс-изомером олеиновой кислоты является элаидиновая кислота, которая плавится при температуре 19-21 °C. Двойная связь в молекуле олеиновой кислоты делает её реакционноспособной. Она участвует в различных химических реакциях, таких как гидрогенизация, в процессе которой олеиновая кислота превращается в стеариновую кислоту[5].
C17H33COOH + H2 → C17H35COOH
Также олеиновая кислота может подвергаться окислению, что приводит к прогорканию[5].
3C17H33COOH + 2KMnO4 + 4H2O → 3C17H35O2COOH (9,10-дигидроксистеариновая кислота) + 2MnO2 + 2KOH
2C17H33COOH + 2KMnO4 + 3H2SO4 → 3C8H17COOH (нонановая кислота) + C7H14(COOH)2 (нонандиовая кислота) + K2SO4 + 2MnSO4 + 2H2O
В результате галогенирования, то есть реакции с галогенами, можно определить степень ненасыщенности кислоты[5].
C17H33COOH + Br2 → C17H33Br2COOH (9,10-дибромстеариновая кислота)
Кроме того, олеиновая кислота вступает в реакцию эстерификации, в результате чего образуются триглицериды, которые находят применение в косметике и медицине.[5]
C17H33COOH + C2H5OH → C17H33COOC2H5 + H2O
Также олеиновая кислота участвует в реакции омыления, в результате которой образуются олеаты, используемые в производстве мыла[3].
C17H33COOH + NaOH → C17H33COONa + H2O
Биологические свойства
В организме синтезируется вещество, которое играет важную роль в метаболизме. Оно снижает уровень «плохого» холестерина, сохраняя при этом «хороший». Кроме того, это вещество обладает противовоспалительными свойствами и уменьшает риск сердечно-сосудистых заболеваний и диабета 2 типа. Абсорбция происходит в желудочно-кишечном тракте, после чего вещество транспортируется хиломикронами. Оно может использоваться как источник энергии или для синтеза мембранных липидов[6].
Применение
Олеиновая кислота — многофункциональный компонент с уникальными физико-химическими свойствами, применяемый в пищевой, косметической, фармацевтической, химической, текстильной и кожевенной промышленности, а также в производстве биотоплива[1].
Пищевая промышленность — олеиновая кислота улучшает текстуру и структуру продуктов, стабилизирует их и продлевает срок хранения. Она является основным компонентом оливкового масла, полезного для здоровья и снижающего риск сердечно-сосудистых заболеваний[1].
Косметическая промышленность — олеиновая кислота увлажняет кожу, улучшает её барьерные функции и консистенцию косметических продуктов. Она также используется в шампунях и средствах для ухода за волосами[1].
Фармацевтическая промышленность. В фармацевтике олеиновая кислота служит основой для мазей, кремов, суппозиториев и инъекций, обеспечивая биодоступность жирорастворимых веществ. Её противовоспалительные и антибактериальные свойства применяются в дерматологии[1].
Химическая промышленность — олеиновая кислота используется для производства мыл, моющих средств, эмульгаторов, смазочных материалов и пластификаторов, диспергируя и стабилизируя эмульсии[1].
Текстильная и кожевенная промышленность: в текстильной промышленности олеиновая кислота придаёт волокнам мягкость и эластичность, а в кожевенной — улучшает гибкость и долговечность изделий[1].
Производство биотоплива. Олеиновая кислота преобразуется в биодизель, снижая выбросы парниковых газов и уменьшая зависимость от ископаемых углеводородов[1].
Уровень опасности и меры предосторожности
Токсичность
Олеиновая кислота (CAS № 112-80-1) — ненасыщенная монокарбоновая кислота, в целом нетоксична, не канцерогенна и не экотоксична. Однако при высоких концентрациях и ненадлежащем обращении она может представлять опасность для здоровья и окружающей среды[7].
Классификация GHS
Раздражение кожи: категория 2. Химические вещества, отнесённые к этой категории, обладают свойством вызывать значительное раздражение кожи при контакте. Это может проявляться в виде покраснения, отёка, зуда или других симптомов. Примером могут служить некоторые кислоты, щёлочи и другие агрессивные соединения[8].
Раздражение глаз: категория 2. Вещества этой категории могут вызывать значительное раздражение глаз при контакте. Это может привести к покраснению, отёку век, слезотечению и другим неприятным ощущениям. Примерами могут служить некоторые чистящие средства, дезинфицирующие растворы и другие химические соединения[8].
Ингаляционная опасность: категория 2 (при термическом разложении). Химические вещества, которые при термическом разложении могут образовывать опасные пары или газы, отнесены к этой категории. Эти пары или газы могут вызывать раздражение дыхательных путей, отравление или другие негативные последствия для здоровья при вдыхании. Примером может служить термическое разложение некоторых органических соединений, которое приводит к образованию токсичных газов[8].
Влияние на водные экосистемы: категория 3. Вещества, отнесённые к этой категории, могут оказывать умеренное негативное воздействие на водные экосистемы. Это может проявляться в виде снижения численности или разнообразия водных организмов, нарушения биохимических процессов в водоёмах и других негативных последствий. Однако степень воздействия может быть недостаточной для отнесения вещества к более высоким категориям[8].
Меры предосторожности
Для обеспечения безопасности при работе необходимо использовать защитную одежду, включая нитриловые, латексные или бутилкаучуковые перчатки. Также важно защитить глаза, надев защитные очки или щиток, особенно при распылении веществ. Если при контакте с кожей средства защиты не предотвратили попадание вещества, следует немедленно промыть кожу водой с мылом. Если возникло раздражение, необходимо обратиться за медицинской помощью.[9].
Дыхательная защита
При проведении работ необходимо обеспечить хорошую вентиляцию помещений. Важно помнить, что при нагревании или распылении веществ следует использовать респираторы типа FFP2 или N95. Особенно это актуально при достижении температур выше 100 °C, чтобы избежать вдыхания паров[10].
Пожарная и термическая безопасность
Температура вспышки вещества составляет около 180 °C. Оно не горит при комнатной температуре, однако поддерживает горение при высоких температурах. Для хранения следует использовать плотно закрытую тару из стекла, нержавеющей стали или устойчивого пластика. Важно избегать попадания света и влаги, чтобы предотвратить окисление. Также необходимо хранить вещество вдали от окислителей, например, пероксидов и нитратов, чтобы исключить возможность нежелательной реакции[11].
Утилизация
Для предотвращения загрязнения необходимо избегать слива каких-либо веществ в канализацию. Вместо этого следует утилизировать их в соответствии с правилами обращения с органическими отходами, соблюдая местные нормы и регламенты.[12].
Примечания
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 1,7 1,8 Олеиновая кислота: что это такое и где применяется. Химплекс. Дата обращения: 19 августа 2025.
- ↑ 2,0 2,1 2,2 Манолов К. Великие химики. Том 1. — Москва: Мир, 1985. — 25 с.
- ↑ 3,0 3,1 Олеиновая кислота. Большая российская энциклопедия (13 января 2023). Дата обращения: 20 августа 2025.
- ↑ Глинка Н. Л. Общая химия : учебник для бакалавров. — М.: Юрайт, 2013. — 898 с. — ISBN 978-5-9916-2901-0.
- ↑ 5,0 5,1 5,2 5,3 Олеиновая кислота. Acetyl. Дата обращения: 20 августа 2025.
- ↑ Олеиновая кислота. Polismed.com. Дата обращения: 20 августа 2025.
- ↑ Олеиновая кислота. Ataman chemicals. Дата обращения: 20 августа 2025.
- ↑ 8,0 8,1 8,2 8,3 Сонина О. Н. Как правильно читать маркировку, предупреждающую о химических опасностях Часть1. Согласованная на глобальном уровне система классификации и маркировки химических веществ (СГС). Портал безопасности (18 февраля 2025). Дата обращения: 20 августа 2025.
- ↑ Химическая безопасность: защита работника от негативного воздействия растворов кислот и щелочей. Учебный центр ЮТМ (9 июля 2024). Дата обращения: 20 августа 2025.
- ↑ Защита органов дыхания работника от воздействия химических факторов (токсичных веществ). Учебный центр ЮТМ (9 июля 2024). Дата обращения: 20 августа 2025.
- ↑ Олеиновая кислота (элаиновая кислота, цис-9-октадеценовая кислота). Фастех. Дата обращения: 20 августа 2025.
- ↑ Утилизация кислот: серной, соляной и других, опасность хранения, алгоритм как утилизировать и методы переработки в быту и на предприятиях. Промэкосервис. Дата обращения: 20 августа 2025.
- Страницы, использующие волшебные ссылки ISBN
- Химические вещества по алфавиту
- Химические вещества без указания химической формулы
- Химические вещества без указания молярной массы
- Химические вещества без указания плотности
- Проект:Шаблоны статей
- Одноосновные карбоновые кислоты
- Жирные кислоты
- Непредельные карбоновые кислоты
