Стеариновая кислота
| Стеариновая кислота | |
|---|---|
  | |
 | |
| Общие | |
| Систематическое наименование |
Октадекановая кислота |
| Традиционные названия | Стеариновая кислота |
| Хим. формула | С17Н35СООН |
| Физические свойства | |
| Состояние | кристаллическое вещество |
| Молярная масса | 284 г/моль г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 69,2—69,9 °C |
| • кипения | 232 °C |
| Оптические свойства | |
| Показатель преломления | 1,4296 |
| Классификация | |
| Рег. номер CAS | 64-19-7 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Стеари́новая кислота́ (октадекановая кислота) — это одноосновная насыщенная жирная карбоновая кислота с брутто-формулой С18Н36О2. Её сокращённая формула записывается как С17Н35СООН или СН3(СН2)16СООН. Это соединение входит в состав животных и растительных жиров, где выполняет важнейшие энергетические и пластические функции[1]. Впервые стеариновая кислота была выделена в 1816 году из свиного жира французским химиком Мишель-Эжен Шеврёлем. Её природными источниками служат разнообразные жиры, включая сало[2].
История открытия
В 1811 году французский химик Луи Никола Воклен принёс в лабораторию образец прогорклого жира и предложил своему ученику Мишелю Эжену Шеврёлю сделать его анализ. Занявшись этой темой, Шеврёль в результате стал основоположником химии жиров. В 1816 году он обнаружил стеариновую кислоту среди других кислот в составе свиного сала. В 1820-х годах Шеврёль открыл способ извлечения стеариновой кислоты из жиров животного происхождения[2].
Свойства
Химическое строение
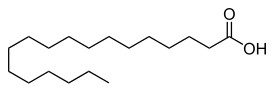
Стеариновая кислота — одноосновная насыщенная (предельная) карбоновая кислота. Химическая формула соединения СН3(СН2)16COOH. Кислота состоит из линейного углеводородного остатка из 17 атомов углерода, связанного с карбоксильной группой (–СООН). Наличие одинарных связей в углеводородном скелете молекулы способствует высокой стабильности кислоты и более высокой температуре плавления по сравнению с непредельными карбоновыми кислотами, содержащими такое же число атомов углерода в углеводородном радикале[3].
Физические свойства
Стеариновая кислота представляет собой бесцветное кристаллическое вещество со слабым характерным запахом стеарина. Её температура плавления составляет 69,2—69,9 °С[4]. Кислота практически нерастворима в воде, но хорошо растворяется в горячем этиловом спирте и диэтиловом эфире[5].
Химические свойства
Стеариновая кислота проявляет типичные свойства карбоновых кислот. Она взаимодействует со щелочами с образованием солей — стеаратов:
C17H35COOH + NaOH → C17H35COONa + H2O
Вступает реакцию этерификации со спиртами, образуя сложные эфиры:
C17H35COOH + C4H9OH ⇌ C17H35COOC4H9 + H2O (в присутствии концентрированной серной кислоты H2SO4)
Стеариновая кислота способна восстанавливаться до стеарилового спирта[6]:
C17H35COOH + 2[H] → C17H35CH2OH (или C18H37OH)
Способы получения
В промышленности стеариновую кислоту получают гидролизом животных жиров и растительных масел. Процесс включает нагревание исходных жиров в водном гидроксиде натрия, в результате чего образуется стеарат натрия и глицерин. Полученная смесь обрабатывается минеральными кислотами, такими как серная или соляная кислоты, с последующим выделением стеариновой кислоты методом фракционной перегонки[7].
Стеариновую кислоту можно получить гидрированием олеиновой кислоты (С17Н33СООН)[7]:
С17Н33СООН + Н2 → С17Н35СООН (катализатор никель или палладий, t = 160 °С, р = 25 бар)
Применение
В промышленности
Стеариновая кислота ― дифильная молекула с полярной карбоксильной группой, которая взаимодействует с водой, и неполярной углеводородной цепью, обеспечивающей растворимость в неполярных средах. Благодаря этому она широко используется как поверхностно-активное вещество для стабилизации суспензий и полимеров. Полярная «голова» молекулы устремляется к воде, тогда как неполярный «хвост» создаёт барьер, предотвращающий слипание капель, что стабилизирует смесь[8].
Стеариновую кислоту применяют совместно с пальмитиновой кислотой (С15Н31СООН) при производстве свечей. Её соли, такие как стеарат натрия и калия, находят применение в изготовлении твёрдых и жидких мыл[4]. В органическом синтезе вещество используется для получения стеарилового спирта (С18Н37ОН) и стерамиламина (C18H37NH2)[9].
В фармацевтике и косметике стеариновая кислота применяется в качестве компонентов кремов, мазей и средств смягчения резиновых изделий[9]. Производные стеариновой кислоты применяются в создании клеевых паст, текстильных эмульсий, стабилизаторов для пищевых продуктов. Например, стеарат кальция используется как загуститель смазок, матирующая добавка для лаков[9], а стеарат цинка — в производстве каучука и пластмасс. Стеарат меди находит применение в бронзировании гипса[10]. Многофункциональность стеариновой кислоты позволяет использовать её в производстве резины в качестве диспергатора наполнителей и активатора вулканизации[10].
В науке
В аналитической химии стеариновая кислота применяется при нефелометрическом определении кальция, магния и лития, а также в качестве жидкой фазы в распределительной газо-жидкостной хроматографии. Стеариновую кислоту добавляют в состав полировальных паст для обработки металлических поверхностей[10].
Нахождение в природе, биологическое значение
Стеариновая кислота встречается в природе в значительных количествах. Её содержание превышает 25 % от общей массы в накопительных жирах некоторых млекопитающих, овечьего жира, а также в растительных жирах тропических растений, таких как масло какао[11]. Окисление стеариновой кислоты осуществляется в митохондриях клеток через стандартный процесс β-окисления жирных кислот[5].
Примечания
- ↑ Иоффе, Д. В. Стеариновая кислота // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский. — 3-е изд. — М. : Советская энциклопедия, 1985. — Т. 24 : Сосудистый шов — Тениоз. — С. 233. — 544 с. : ил.
- ↑ 2,0 2,1 Энциклопедия для детей. Химия / Ред. коллегия: М. Аксёнова, И. Леенсон, С. Мартынова и др.. — 2-е изд. — М.: Мир энциклопедий Аванта+, 2007. — Т. 17. — С. 497. — 656 с. — ISBN 978-5—98986—036—4 (т. 17).
- ↑ Стеариновая кислота: структура, характеристики и применение. Ведущая компания Шамми. Дата обращения: 27 февраля 2025.
- ↑ 4,0 4,1 Левитина Т. П. Справочник по органической химии: Учебное пособие. — СПб.: Паритет, 2002. — С. 285. — 448 с. — ISBN 5—93437—090—1.
- ↑ 5,0 5,1 А. Кузин. Стеариновая кислота. Большая медицинская энциклопедия.
- ↑ Левитина Т. П. Справочник по органической химии: Учебное пособие. — СПб.: Паритет, 2002. — С. 280—282. — 448 с. — ISBN 5-93437-090-1.
- ↑ 7,0 7,1 Химия. Большой энциклопедический словарь / Гл. ред. И. Л. Кнунянц. — 2- изд. — М.: Научное издательство «Большая Российская энциклопедия», 1998. — С. 541. — 792 с. — ISBN 5—85270—253—6 (БРЭ).
- ↑ Стеариновая кислота: свойства и применение. ForplastTrading. Дата обращения: 24 февраля 2025.
- ↑ 9,0 9,1 9,2 Рудаков, О. Б. Стеариновая кислота. Научно-образовательный портал «Большая российская энциклопедия» (26 октября 2022). Дата обращения: 3 февраля 2025.
- ↑ 10,0 10,1 10,2 Стеариновая кислота. Пропласт. Дата обращения: 24 февраля 2025.
- ↑ Грандберг И. И. Органическая химия: Учеб. для студ. вузов, обучающихся по агроном. спец.. — 5-е изд, стереотип. — М.: Дрофа, 2002. — С. 394. — 672 с. — ISBN 5—7107—6129—X.
Данная статья имеет статус «готовой». Это не говорит о качестве статьи, однако в ней уже в достаточной степени раскрыта основная тема. Если вы хотите улучшить статью — правьте смело! |
Данная статья имеет статус «проверенной». Это говорит о том, что статья была проверена экспертом |
