Стенокардия
Стенокарди́я (др.-греч. στενός, узкий, тесный; слабый + др.-греч. καρδία — сердце, лат. angina pectoris, а́нгина пе́кторис) — клинический синдром, характеризующийся приступообразными болевыми ощущениями или дискомфортом в области грудной клетки, возникающими вследствие острого дисбаланса между потребностью миокарда в кислороде и его доставкой через коронарные артерии[1]. Данное состояние является одним из наиболее распространённых проявлений ишемической болезни сердца и затрагивает миллионы людей по всему миру.
Происхождение термина
Современное медицинское наименование заболевания берёт своё начало из древнегреческого языка, где слово «στενός» означает «узкий, тесный, слабый», а «καρδία» переводится как «сердце». Латинский эквивалент angina pectoris буквально означает «удушение груди», что точно отражает субъективные ощущения пациентов во время приступа.
В отечественной медицинской литературе долгое время использовался термин «грудная жаба». Сегодня он считается устаревшим[2].
История изучения
- Древние корни понимания болезни
Представления о сердечных болях, схожих со стенокардией, существовали ещё в древности. В традиционной индийской медицине подобное состояние описывалось под названием «hritshoola» и было детально охарактеризовано выдающимся хирургом древности Сушрутой в VI веке до нашей эры[3]. Эти ранние описания демонстрируют, что клинические проявления коронарной недостаточности были знакомы врачам различных цивилизаций задолго до формирования современных представлений о патофизиологии сердечно-сосудистых заболеваний.
- Становление европейской клинической школы
Фундаментальный вклад в понимание стенокардии внёс британский врач Уильям Хеберден, который в 1768 году представил первое систематическое клиническое описание данного синдрома[4]. Его наблюдения заложили основу для дальнейшего изучения коронарной патологии и до сих пор остаются актуальными в клинической практике. В начале XX века тяжёлые формы стенокардии рассматривались врачами как предвестники неминуемой смерти, однако развитие современной медицины кардинально изменило прогноз заболевания.
- Терапевтические достижения
Революционным моментом в лечении стенокардии стало внедрение нитроглицерина, который используется для симптоматического облегчения приступов с 1879 года[5]. Это открытие положило начало эре фармакологической терапии коронарной недостаточности и послужило отправной точкой для разработки множества современных антиангинальных препаратов.
Причины возникновения и механизмы развития
Основы патофизиологии
Стенокардия развивается в результате острого несоответствия между потребностями сердечной мышцы в кислороде и возможностями коронарного кровотока обеспечить эти потребности[6]. При недостаточном поступлении кислорода в кардиомиоцитах нарушаются процессы аэробного метаболизма, что приводит к накоплению недоокисленных продуктов обмена веществ, включая молочную, пировиноградную, угольную и фосфорную кислоты. Именно эти метаболические нарушения становятся причиной характерных болевых ощущений.
Механизм развития ишемии может реализовываться через различные пути. Снижение кровотока может быть вызвано стенозом, спазмом или острой окклюзией коронарных артерий. Сопротивление кровеносных сосудов играет критическую роль — даже небольшое уменьшение радиуса артерии приводит к значительному снижению кровотока, поскольку скорость кровотока пропорциональна четвёртой степени радиуса сосуда. Кроме того, снижение кислородтранспортной способности крови при тяжёлой анемии или длительном курении также может привести к развитию ишемии миокарда при сохранной проходимости коронарных артерий.
Атеросклеротические изменения
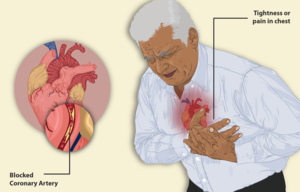
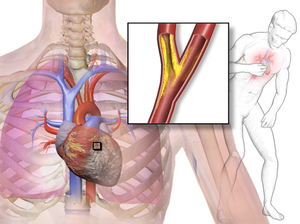
Наиболее частой причиной стенокардии является атеросклероз коронарных артерий, при котором формирующиеся атеросклеротические бляшки сужают просвет сосудов и ограничивают кровоток к миокарду. Значительно реже встречаются инфекционные и инфекционно-аллергические поражения венечных артерий.
Атеросклеротические изменения могут проявляться в виде стабильных стенозов, острых окклюзий вследствие тромбоза или эмболии. Кроме того, они могут быть связаны со спазмом коронарных сосудов[7].
Микроваскулярные нарушения
Особую группу составляют пациенты с микроваскулярной стенокардией, также известной как синдром X, при которой типичные ангинозные боли возникают на фоне нормальных или минимально изменённых эпикардиальных коронарных артерий[8]. В основе данного состояния лежит эндотелиальная дисфункция и нарушение функции мелких интрамиокардиальных сосудов, что приводит к локальной ишемии миокарда без видимых изменений на коронарографии.
Патофизиология микроваскулярной стенокардии остаётся сложной и до конца не изученной, но накапливается всё больше доказательств участия множественных механизмов. Эндотелиальная дисфункция проявляется снижением продукции эндогенных вазодилататоров, усилением воспалительных процессов, изменениями в метаболизме адипокинов и повышенной активацией тромбоцитов. Маленькие интрамиокардиальные артериолы подвергаются констрикции, что делает ишемическую боль менее предсказуемой по сравнению с типичной эпикардиальной коронарной болезнью.
Ранее микроваскулярная стенокардия считалась относительно доброкачественным состоянием, однако современные данные изменили это представление. Исследования показывают, что данная патология является частью патофизиологии ишемической болезни сердца и может объяснять более высокую частоту стенокардии у женщин по сравнению с мужчинами, а также их предрасположенность к ишемии и острым коронарным синдромам при отсутствии обструктивной коронарной болезни.
Классификация и клинические формы
Систематизация стенокардии
Современная классификация ишемической болезни сердца была разработана в СССР в 1984 году на основе рекомендаций экспертов Всемирной организации здравоохранения 1979 года[9]. Данная систематизация предусматривает выделение стабильной и нестабильной форм стенокардии с детальной характеристикой каждого варианта течения заболевания.
Стабильная стенокардия напряжения классифицируется по функциональным классам от I до IV в зависимости от переносимости физических нагрузок:
- I функциональный класс — приступы возникают только при значительных нагрузках, превышающих обычную повседневную активность.
- II класс — некоторое ограничение обычной физической активности.
- III класс — выраженное ограничение физической активности.
- IV класс — невозможность выполнения любой физической нагрузки без дискомфорта.
Нестабильные коронарные синдромы
Нестабильная стенокардия определяется как внезапное изменение характера болевого синдрома, его утяжеление или появление приступов в состоянии покоя. Выделяют несколько основных вариантов[10]:
- впервые возникшая (в течение предыдущих 28-30 дней);
- прогрессирующая (усиление частоты, интенсивности или продолжительности приступов);
- ранняя постинфарктная;
- спонтанная вазоспастическая.
Классификация по остроте возникновения включает три класса:
- I — недавнее начало тяжёлой стенокардии с анамнезом менее 2 месяцев.
- II — подострая стенокардия покоя в течение месяца, но не в последние 48 часов.
- III — острая стенокардия покоя в течение последних 48 часов.
Особые варианты течения
Вариантная стенокардия Принцметала представляет собой особую форму заболевания, которая возникает у пациентов с нормальными коронарными артериями или незначительным атеросклерозом. Она обусловлена спазмом венечных сосудов[11].
Данный вариант чаще встречается у молодых женщин и характеризуется приступами в ночное время или ранние утренние часы. Статистические данные показывают, что 64 % всех случаев нестабильной стенокардии происходят в период с 22:00 до 08:00, когда пациенты находятся в состоянии покоя.
Клинические проявления
Характеристика болевого синдрома
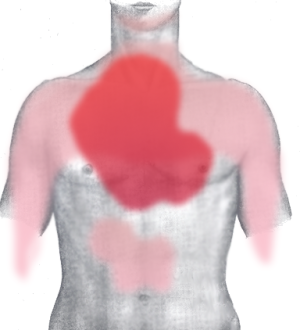
Типичный приступ стенокардии проявляется ощущением дискомфорта давящего, сжимающего или жгучего характера в области грудины. Пациенты часто описывают свои ощущения, прикладывая сжатый кулак или открытую ладонь к груди, что получило название «симптом сжатого кулака».
Болевые ощущения обычно возникают внезапно при физической нагрузке, эмоциональном стрессе, после обильного приёма пищи или на холоде. Они могут продолжаться от одной до пятнадцати минут[12].
Паттерны распространения боли
Характерной особенностью стенокардии является иррадиация болевых ощущений в определённые анатомические области. Наиболее часто боль распространяется в левое плечо и внутреннюю поверхность левой руки, область шеи, нижнюю челюсть.
Реже встречается иррадиация в правое плечо, межлопаточную область спины или эпигастральную зону. Боль может сопровождаться диспептическими расстройствами в виде изжоги, тошноты или кишечных колик[13].
Атипичные формы проявления
Особую сложность для диагностики представляют атипичные варианты стенокардии. У женщин, пожилых пациентов и больных сахарным диабетом клинические проявления могут включать одышку, тошноту, эпигастральный дискомфорт, ощущение жжения или общую слабость без типичной загрудинной боли[14]. Исключительно редко болевой синдром локализуется исключительно в эпигастральной области или даже в области головы, что значительно затрудняет своевременную диагностику.
Некоторые пациенты испытывают так называемые автономные симптомы, связанные с активацией вегетативной нервной системы: бледность кожных покровов, повышенное потоотделение, тошноту и рвоту. Эти проявления особенно характерны для приступов стенокардии у лиц пожилого возраста и могут доминировать в клинической картине, затрудняя дифференциальную диагностику с другими заболеваниями.
Боль при стенокардии обычно не бывает острой, колющей или связанной с дыханием. Характерной особенностью является то, что антациды и простые анальгетики не приносят облегчения при истинной стенокардитической боли. Если загрудинный дискомфорт провоцируется физической нагрузкой, исчезает в покое и купируется нитроглицерином, вероятность стенокардии значительно возрастает.
Факторы риска
Основные управляемые факторы
Курение табака является одним из наиболее значимых факторов риска развития стенокардии. Исследования показывают, что курильщики с ишемической болезнью сердца имеют значительно повышенный уровень активности симпатической нервной системы по сравнению с некурящими пациентами[15]. Кроме того, важными управляемыми факторами риска являются:
- сахарный диабет;
- дислипидемия;
- артериальная гипертензия;
- ожирение с индексом массы тела 30 кг/м² и более;
- гиподинамия;
- хронический психосоциальный стресс.
Неуправляемые факторы
К неуправляемым факторам риска относится возраст: 45 лет и старше для мужчин и 55 лет и старше для женщин. В эту же группу входит отягощённая наследственность по сердечно-сосудистым заболеваниям.
Семейный анамнез считается положительным при развитии коронарной патологии у мужчин моложе 55 лет. Для женщин этот показатель определяется возрастом моложе 65 лет[16].
Сопутствующие заболевания
Ряд патологических состояний может спровоцировать развитие стенокардии или усугубить её течение. К ним относятся хроническая почечная недостаточность с микроальбуминурией или снижением скорости клубочковой фильтрации менее 60 мл/мин, полицитемия, гипотермия, нарушения объёма циркулирующей крови, заболевания пищевода, гастроэзофагеальная рефлюксная болезнь, гипертиреоз, гипоксемия различного генеза и неконтролируемая артериальная гипертензия.
Анемия может служить как фактором, провоцирующим стенокардию, так и проявлением основного онкологического заболевания[17]. Это требует дополнительного обследования пациентов с впервые выявленной коронарной симптоматикой на фоне железодефицитного состояния.
Особое внимание следует уделять кардиальным причинам, которые могут имитировать стенокардию или усугублять её течение. Брадиаритмии, тахиаритмии, гипертрофическая кардиомиопатия и клапанные пороки сердца могут создавать дополнительную нагрузку на миокард или нарушать его кровоснабжение. У пациентов с выраженной гипертрофией левого желудочка, вызванной стенозом аортального клапана, аортальной регургитацией или дилатационной кардиомиопатией, стенокардитические боли могут возникать даже при отсутствии значимых изменений в коронарных артериях.
Диагностика
Электрокардиографические методы
Электрокардиография в покое является обязательным методом обследования всех пациентов с подозрением на стенокардию и должна выполняться в 12 стандартных отведениях. Хотя результаты ЭКГ покоя остаются нормальными примерно у половины больных стенокардией, данное исследование позволяет выявить признаки перенесённого инфаркта миокарда, нарушения реполяризации, гипертрофию левого желудочка и различные нарушения ритма сердца.
Нагрузочные ЭКГ-тесты (тредмил-тест, велоэргометрия) являются основными методами функциональной диагностики стенокардии[18]. Основным диагностическим критерием служит горизонтальная или косонисходящая депрессия сегмента ST величиной 0,1 мВ и более, сохраняющаяся не менее 0,06-0,08 секунды после точки J в одном или нескольких отведениях ЭКГ.
Визуализирующие методы
Эхокардиография в покое помогает исключить другие причины болей в груди, такие как клапанные пороки сердца или гипертрофическую кардиомиопатию, а также оценить функцию желудочков и размеры полостей сердца. Стресс-эхокардиография в сочетании с физической или фармакологической нагрузкой представляет собой альтернативу сцинтиграфии миокарда[19].
Сцинтиграфия миокарда с использованием изотопов таллия-201 или технеция-99 проводится в сочетании с физической нагрузкой или фармакологическими пробами при невозможности выполнения физических упражнений. Современные методы визуализации включают позитронно-эмиссионную томографию, магнитно-резонансную томографию сердца и трансторакальную допплеровскую эхокардиографию.
Лабораторная диагностика
При подозрении на нестабильную стенокардию необходимо определение биохимических маркёров повреждения миокарда, в первую очередь тропонина или МВ-фракции креатинфосфокиназы. Повышение уровня этих показателей указывает на наличие острого коронарного синдрома[20].
Всем пациентам показано исследование липидного профиля (общий холестерин, липопротеиды высокой и низкой плотности, триглицериды) для оценки сердечно-сосудистого риска. Определение уровня креатинина необходимо для оценки функции почек, а исследование глюкозы натощак и гликированного гемоглобина — для выявления сахарного диабета.
Клинический анализ крови помогает выявить сопутствующие заболевания, которые могут провоцировать ишемию миокарда. Снижение уровня гемоглобина указывает на анемию, изменения лейкоцитарной формулы могут свидетельствовать о воспалительных процессах, эритремии или лейкозе. При наличии клинических признаков дисфункции щитовидной железы определяют уровень тиреотропного гормона и свободного тироксина в крови.
Медикаментозное лечение
Антиангинальная терапия первой линии
Бета-адреноблокаторы являются препаратами первого выбора для лечения стенокардии благодаря их способности эффективно купировать приступы и улучшать прогноз заболевания[21]. Механизм их действия основан на снижении потребности миокарда в кислороде за счёт уменьшения частоты сердечных сокращений и артериального давления. Предпочтение отдаётся кардиоселективным препаратам (метопролол, бисопролол, атенолол), которые реже вызывают побочные эффекты.
Эффективность терапии оценивается по достижению целевых значений частоты сердечных сокращений: менее 60 ударов в минуту в покое и менее 110 ударов в минуту при максимальной физической активности. Побочные эффекты включают похолодание конечностей, симптомную брадикардию, обострение бронхиальной астмы и хронической обструктивной болезни лёгких, нарушения половой функции, кошмарные сновидения и общую слабость.
Блокаторы кальциевых каналов
Блокаторы кальциевых каналов подразделяются на две основные группы: недигидропиридиновые (верапамил, дилтиазем) и дигидропиридиновые (нифедипин, амлодипин, левамлодипин) производные. Все препараты данной группы обладают антиангинальным действием, снижая рабочую нагрузку на сердце и его потребность в кислороде[22].
Производные дигидропиридина можно комбинировать с бета-адреноблокаторами у пациентов с недостаточным эффектом монотерапии. Комбинация недигидропиридиновых блокаторов кальциевых каналов с бета-блокаторами не рекомендуется из-за риска чрезмерной брадикардии. Наиболее частым побочным эффектом являются периферические отёки нижних конечностей.
Органические нитраты
В клинической практике применяются три основных препарата группы нитратов: нитроглицерин, изосорбида динитрат и изосорбида мононитрат. Классификация предусматривает деление на формы короткого действия (менее 1 часа), умеренного пролонгированного действия (менее 6 часов) и значительного пролонгированного действия (6-24 часа)[23].
При стенокардии I функционального класса назначаются нитраты короткого действия для профилактического приёма за 5-10 минут до предполагаемой физической нагрузки. При более тяжёлых функциональных классах используются пролонгированные формы с обязательным соблюдением безнитратного периода продолжительностью 5-6 часов для предотвращения развития толерантности.
Основными побочными эффектами нитратов являются головная боль и гиперемия лица, обусловленные расширением сосудов. Передозировка может привести к ортостатической гипотензии и рефлекторной тахикардии.
Толерантность к нитратам развивается при длительном приёме пролонгированных форм без соблюдения безнитратного интервала. Механизм развития толерантности связан с истощением внутриклеточных запасов сульфгидрильных групп, необходимых для превращения нитратов в оксид азота. Для предотвращения толерантности используется молсидомин — препарат с механизмом действия, похожим на органические нитраты, но к которому толерантность не развивается.
Инновационные антиишемические препараты
Ивабрадин представляет собой первый в своём классе ингибитор If-каналов избирательного и специфического действия[24]. В отличие от других пульсурежающих средств, ивабрадин не влияет на сократимость миокарда, диастолическую функцию, периферическое сосудистое сопротивление и артериальное давление. Стартовая дозировка составляет 5 мг дважды в день в течение двух недель с последующим увеличением до 7,5 мг дважды в день.
Никорандил представляет собой комбинированное лекарственное средство, объединяющее свойства стимулятора АТФ-чувствительных калиевых каналов с нитратоподобными характеристиками. Данный медикамент обеспечивает вазодилатацию как поражённых, так и интактных участков коронарного русла при стандартном режиме дозирования 20 мг с двукратным суточным приёмом.
Ранолазин функционирует в качестве избирательного блокатора поздней натриевой проводимости, что приводит к торможению потенциал-зависимого транспорта кальция и снижению повреждающего влияния на миокардиальные клетки. Лекарственное средство в режиме дозирования 500—1500 мг с двукратным приёмом либо в пролонгированной форме 750—1000 мг дважды в сутки результативно усиливает базисную терапию, способствуя повышению переносимости нагрузочных проб и урежению ангинозных эпизодов. К нежелательным реакциям относятся констипация, вестибулярные расстройства, диспептические явления и астенический синдром.
Триметазидин принадлежит к классу цитопротективных средств, обеспечивающих стабилизацию клеточного энергетического гомеостаза и предотвращающих электролитные сдвиги в условиях гипоксии. Механизм реализуется через активацию гликолиза и подавление β-окисления липидов, при этом терапевтическая значимость препарата остаётся дискутабельной ввиду недостаточно изученных фармакодинамических особенностей.
Антитромботическая терапия
Антиагрегантные препараты — аспирин рекомендуется к постоянному применению у всех пациентов со стенокардией в суточной дозировке 75-150 мг при отсутствии медицинских ограничений[25]. Дозирование следует поддерживать на минимальном терапевтически значимом уровне, так как повышение количества препарата ассоциируется с возрастанием вероятности гастроинтестинальных нежелательных явлений, в том числе геморрагических осложнений и ульцерогенного воздействия.
В случаях непереносимости ацетилсалициловой кислоты альтернативой служит клопидогрел, превосходство которого в плане эффективности и безопасности относительно желудочно-кишечного тракта подтверждено в контролируемых клинических испытаниях. Комбинирование эзомепразола в суточной дозе 80 мг с аспирином обеспечивает более надёжную защиту от повторных пептических кровотечений по сравнению со стратегией замещения на клопидогрел.
Липидкорригирующая терапия
Препараты группы статинов (блокаторы 3-гидрокси-3-метилглутарил-коэнзим А редуктазы) представляют основу медикаментозной коррекции нарушений липидного обмена и обладают способностью стабилизировать имеющиеся атеросклеротические образования[26]. Терапевтические цели предусматривают достижение концентрации общего холестерина ниже 4,5 ммоль/л (175 мг/дл) и холестерина фракции липопротеинов низкой плотности менее 2,5 ммоль/л (100 мг/дл).
Хирургические методы лечения
Прямая реваскуляризация
Операция коронарного шунтирования заключается в формировании альтернативного пути кровотока путём соединения аорты с венечной артерией в области дистальнее участка сужения[27]. Для создания шунтов применяются аутологичные сосудистые трансплантаты — собственные венозные и артериальные сосуды больного, причём оптимальным выбором признаётся использование внутренней грудной артерии для маммарно-коронарного анастомоза.
Эндоваскулярные вмешательства
Менее инвазивной альтернативой открытого хирургического вмешательства служит процедура чрескожной коронарной ангиопластики с последующим стентированием. Данная методика предполагает механическое расширение стенозированного сегмента венечной артерии при помощи раздуваемого баллона с дальнейшей установкой специального каркаса — стента. Изолированная баллонная дилатация без имплантации стента утратила своё клиническое значение ввиду неудовлетворительных отдалённых результатов.
Применяемые стенты классифицируются на простые металлические конструкции без покрытия (bare metal stent^[en]^) и стенты с лекарственным покрытием, содержащие антипролиферативные препараты (drug eluting stent^[en]^). Выбор оптимальной стратегии реваскуляризации осуществляется персонализированно на основании данных коронарной ангиографии с анализом анатомических особенностей поражения, сократительной способности миокарда левого желудочка и коморбидного фона пациента[28].
Особенности ведения женщин
- Гендерные различия в патофизиологии
Патофизиология стенокардии у женщин имеет существенные отличия от таковой у мужчин, что связано с большей распространённостью необструктивной коронарной болезни сердца у представительниц женского пола[29]. Микроваскулярная стенокардия встречается почти у половины женщин с ишемией миокарда при отсутствии значимых стенозов эпикардиальных коронарных артерий.
- Диагностические особенности
Женщины с ишемией миокарда часто имеют нетипичные симптомы, включающие сердцебиение, тревожность, общую слабость и быструю утомляемость, что может затруднять своевременную диагностику. Для подтверждения диагноза микроваскулярной стенокардии может потребоваться катетеризация с оценкой микроциркуляторного ответа на введение аденозина или ацетилхолина и измерение коронарного и фракционного резерва кровотока[30].
Прогноз и профилактика
Современные возможности прогнозирования
В настоящее время стенокардия не рассматривается как фатальное заболевание благодаря достижениям современной медицины. Пациенты среднего возраста с умеренной и тяжёлой стенокардией II—IV функциональных классов имеют пятилетнюю выживаемость около 92 %[31].
Тем не менее заболевание остаётся серьёзной угрозой для жизни. Через пять лет после установления диагноза примерно 4,8 % пациентов умирают от осложнений ишемической болезни сердца.
Модификация образа жизни
Ключевыми компонентами профилактики прогрессирования заболевания являются отказ от курения, поддержание умеренной физической активности и соблюдение диеты с ограничением потребления соли и насыщенных жиров при регулярном употреблении фруктов, овощей и рыбы[32]. Физические упражнения представляют собой эффективный долгосрочный метод лечения стенокардии, однако предпочтение следует отдавать мягким устойчивым нагрузкам, а не интенсивным кратковременным упражнениям.
Отказ от курения приносит как краткосрочные, так и долгосрочные преимущества. Исследования показывают, что риск ишемической болезни сердца, инсульта и заболеваний периферических сосудов снижается в течение 1-2 лет после прекращения курения. У курящих мужчин моложе 60 лет после первого приступа стенокардии распространённость ангинозных эпизодов через год была на 40 % меньше у тех, кто бросил курить, по сравнению с продолжающими курение.
Рациональная диетотерапия должна включать ограничение общей калорийности при избыточной массе тела, снижение потребления насыщенных жиров до менее 7 % от общей калорийности, ограничение холестерина до 200 мг в сутки и трансжиров до минимума. Рекомендуется увеличение потребления омега-3 жирных кислот, содержащихся в рыбе, и растворимой клетчатки. Регулярное рутинное консультирование взрослых врачами для улучшения диеты и увеличения физической активности показало лишь небольшие изменения в поведении, поэтому предпочтение следует отдавать селективному консультированию пациентов, наиболее готовых к изменению образа жизни.
Эпидемиология
По состоянию на 2010 год, стенокардией, обусловленной ишемической болезнью сердца, страдает примерно 112 миллионов человек во всём мире, что составляет 1,6 % глобального населения, с незначительным преобладанием среди мужчин (1,7 %) по сравнению с женщинами (1,5 %)[33]. В Соединённых Штатах насчитывается 10,2 миллиона пациентов со стенокардией, при этом ежегодно регистрируется около 500 тысяч новых случаев заболевания.
Стенокардия чаще является первым проявлением ишемической болезни сердца у женщин, чем у мужчин. Распространённость заболевания увеличивается с возрастом, при этом средний возраст дебюта составляет 62,3 года. В возрастной группе 45-54 лет частота встречаемости стенокардии составляет около 2-5 %, тогда как в возрасте 65-74 лет этот показатель возрастает до 10-20 %.
Литература
- Фадеев П.А. Стенокардия. — М.: Мир и Образование, Оникс, 2012. — С. 192.
- Шимкевич В.М., Догель А.С., Тарханов И.Р., Островский В.М. Сердце. — СПб., 1890–1907. — (Энциклопедический словарь Брокгауза и Ефрона).
- White P.D. Heart Disease. — 1st ed.. — New York: Macmillan, 1931. — P. 929.
Примечания
- ↑ Белов, Н. И. Справочник медицинской сестры по уходу / под ред. Н. Р. Палеева. — М.: Медицина, 1980. — С. 336. — ISBN 978-5-225-08901-4.
- ↑ Лазарева, Н. В. Стенокардия: современные подходы к диагностике и лечению. — М.: ГЭОТАР-Медиа, 2019. — С. 128. — ISBN 978-5-9704-5123-8.
- ↑ G. Dwivedi, S. Dwivedi. Sushruta – the Clinician – Teacher par Excellence // The Indian Journal of Chest Diseases and Allied Sciences. — 2007. — Vol. 49. — P. 243–244.
- ↑ Heberden, W. Some account of a disorder of the breast // Medical transactions. — London: College of Physicians, 1772. — Vol. 2. — P. 59–67.
- ↑ Sneader, W. Drug discovery: a history. — New Jersey: Wiley, 2005. — P. 468. — ISBN 978-0-471-89979-2.
- ↑ Фролов, А. В. Ишемическая болезнь сердца. — СПб.: Элби-СПб, 2018. — С. 224. — ISBN 978-5-93979-394-7.
- ↑ Национальные клинические рекомендации по кардиологии / под ред. Ю. Н. Беленкова. — 3-е изд. — М.: Силицея-Полиграф, 2010. — С. 592. — ISBN 978-5-94869-096-2.
- ↑ G. A. Lanza, F. Crea. Primary coronary microvascular dysfunction: clinical presentation, pathophysiology, and management // Circulation. — 2010. — Vol. 121, № 21. — P. 2317–2325.
- ↑ Клинические рекомендации по диагностике и лечению стабильной ишемической болезни сердца. — М.: Издательство «Силицея-Полиграф», 2013. — С. 69. — (Российское кардиологическое общество).
- ↑ Бокерия, Л. А. Клинические рекомендации по ведению больных с острым коронарным синдромом без стойких подъёмов сегмента ST на ЭКГ. — М.: НЦССХ им. А. Н. Бакулева РАМН, 2014. — С. 154. — ISBN 978-5-7982-0298-7.
- ↑ Yasue, H. Coronary artery spasm – clinical features, diagnosis, pathogenesis, and treatment // Journal of Cardiology. — 2008. — Vol. 51, № 1. — P. 2–17.
- ↑ Карпов, Ю. А. Стабильная стенокардия: тактика ведения пациентов. — М.: Реафарм, 2003. — С. 256. — ISBN 5-203-01917-X.
- ↑ Гиляревский, С. Р. Современные подходы к лечению больных стенокардией. — М.: МедПрактика-М, 200. — С. 112. — ISBN 5-901654-14-3.
- ↑ Canto, J. G. Symptom Presentation of Women With Acute Coronary Syndromes: Myth vs Reality // Archives of Internal Medicine. — 2007. — Vol. 167, № 22. — P. 2405–2413.
- ↑ Shinozaki, N. Cigarette smoking augments sympathetic nerve activity in patients with coronary heart disease // International Heart Journal. — 2008. — Vol. 49, № 3. — P. 261–272.
- ↑ Сидоренко, Г. И. Ишемическая болезнь сердца. — Минск: Беларусь, 2003. — С. 448. — ISBN 985-01-0401-X.
- ↑ Perera, C. A. Deceitful red-flag: angina secondary to iron deficiency anaemia as a presenting complaint for underlying malignancy // BMJ Case Report. — 2019. — Vol. 12, № 7.
- ↑ Gibbons, R. J. ACC/AHA 2002 guideline update for exercise testing: summary article // Circulation. — 2002. — Vol. 106, № 14. — P. 1883–1892.
- ↑ Аронов Д. М. Функциональные пробы в кардиологии. — 3-е изд. — М.: МЕДпресс-информ, 2007. — С. 328. — ISBN 978-5-98322-320-5.
- ↑ Марцевич, С. Ю. Острый коронарный синдром. — М.: Планида, 2010. — С. 200. — ISBN 978-5-94272-067-4.
- ↑ Tobin, K. J. Stable angina pectoris: what does the current clinical evidence tell us? // The Journal of the American Osteopathic Association. — 2010. — Vol. 110, № 7. — С. 364–370.
- ↑ Метелица, В. И. Справочник по клинической фармакологии сердечно-сосудистых лекарственных средств. — 2-е изд. — М.: Медпрактика-М, 2002. — С. 527. — ISBN 5-901654-08-9.
- ↑ Преображенский, Д. В. Применение нитратов при лечении больных ишемической болезнью сердца. — М.: Информатик, 1998. — С. 64. — ISBN 5-7005-0089-2.
- ↑ Sulfi S. Ivabradine -- the first selective sinus node I(f) channel inhibitor in the treatment of stable angina // International Journal of Clinical Practice. — 2006. — Vol. 60, № 2. — P. 222–228.
- ↑ Antithrombotic Trialists' Collaboration. Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients // BMJ. — 2002. — Vol. 324, № 7329. — P. 71–86.
- ↑ Nissen S. E. Effect of very high-intensity statin therapy on regression of coronary atherosclerosis: the ASTEROID trial // JAMA. — 2006. — Vol. 295, № 13. — P. 1556–1565.
- ↑ Бокерия Л. А. Коронарная хирургия. — 2-е изд. — М.: НЦССХ им. А. Н. Бакулева РАМН, 2009. — С. 712. — ISBN 978-5-7982-0226-0.
- ↑ Жбанов И. В. Миниинвазивная коронарная хирургия. — 2019. — Т. 12. — С. 377–385. — (Кардиология и сердечно-сосудистая хирургия).
- ↑ Shaw L. J. The economic burden of angina in women with suspected ischemic heart disease: results from the National Institutes of Health--National Heart, Lung, and Blood Institute--sponsored Women's Ischemia Syndrome Evaluation // Circulation. — 2006. — Vol. 114, № 9.
- ↑ Михеев А. А. Микроваскулярная стенокардия: диагностика и лечение. — М.: Практическая медицина, 2015. — С. 144. — ISBN 978-5-98811-398-2.
- ↑ Boden, W. E. Optimal medical therapy with or without PCI for stable coronary disease // The New England Journal of Medicine. — 2007. — Vol. 356, № 15. — P. 1503–1516.
- ↑ Болдуева С. А. Вторичная профилактика у пациентов с ишемической болезнью сердца после реваскуляризации миокарда. — Доктор.Ру, 2022. — Т. 21. — С. 19–24.
- ↑ Roth G. A. Global, regional, and national burden of cardiovascular diseases for 10 causes, 1990 to 2015 // Journal of the American College of Cardiology. — 2017. — Vol. 70, № 1. — P. 1–25.