Билирубин
| Билирубин | |
|---|---|
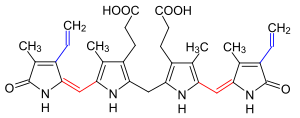
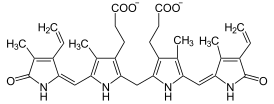  Химическая формула билирубина Химическая формула билирубина | |
| Общие | |
| Хим. формула | C33H36N4O6 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 584,68 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 192 °C |
| Классификация | |
| Рег. номер CAS | 635-65-4 |
| SMILES | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Билируби́н (лат. bilis — желчь и лат. ruber — красный) — ключевой метаболит гемовых соединений, выполняющий множественные биологические функции в организме высших животных.
Данное соединение образуется в результате катаболического расщепления белков, содержащих гем-группы, включая гемоглобин, миоглобин и цитохромы[1]. Характеризуясь сложной тетрапиррольной структурой и уникальными физико-химическими свойствами, билирубин играет важнейшую роль в поддержании клеточного гомеостаза и защитных механизмов организма.
Химическое строение и свойства
Молекулярная структура
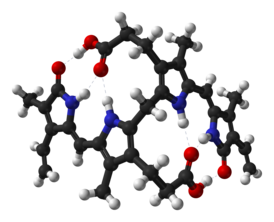
Молекулярная структура билирубина основана на открытой цепи четырёх пиррольных колец, соединённых метиновыми мостиками. Химическая формула C33H36N4O6 отражает сложность данного соединения с молекулярной массой 584,68 г/моль.
В кристаллическом состоянии вещество существует в виде коричневых ромбических образований[2], что обусловлено особенностями межмолекулярного взаимодействия. Структурное родство с фикобилином водорослей и фитохромом растений указывает на эволюционную древность тетрапиррольных пигментов в биологических системах.
Кристаллическая структура билирубина была детально исследована с использованием рентгеноструктурного анализа, что позволило установить точное пространственное расположение атомов и характер водородных связей между молекулами.
Физические свойства и растворимость
Термическая стабильность билирубина характеризуется температурой плавления в диапазоне 192—235 °C, что свидетельствует о прочности кристаллической решётки. Плотность соединения составляет 1,31 г·см-3[2], определяя его физические характеристики в различных средах.
Растворимость билирубина демонстрирует выраженную селективность:
- полная нерастворимость в воде;
- хорошая растворимость в неполярных органических растворителях (бензол, хлороформ, хлорбензол);
- ограниченная растворимость в диэтиловом эфире, глицерине и этаноле.
Способность к селективной растворимости определяется наличием внутримолекулярных водородных связей, которые стабилизируют молекулу в неполярных средах и препятствуют взаимодействию с полярными растворителями.
Воздействие света
Спектральные свойства билирубина определяются поглощением электромагнитного излучения в диапазоне 450—460 нм, соответствующем синей области видимого спектра. Фотохимическая трансформация под воздействием света приводит к изомеризации связей, при которой E,Z-изомеры билирубина приобретают повышенную растворимость по сравнению с естественным Z,Z-изомером[3].
Данный механизм лежит в основе фототерапевтических подходов при лечении неонатальной желтухи. Световое воздействие также инициирует превращение билирубина в люмирубин, обладающий улучшенными характеристиками выведения.
Интенсивность фотоизомеризации зависит от длины волны излучения, при этом синий свет оказывается наиболее эффективным для терапевтических целей. Процесс является обратимым, что позволяет молекуле возвращаться к исходной конфигурации в отсутствие светового воздействия.
Образование и превращения
Образование из гема
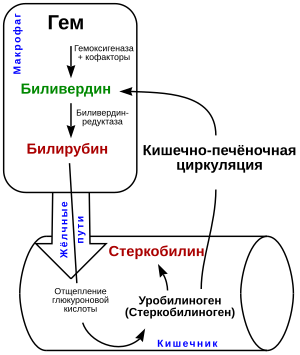
Биосинтетический путь билирубина инициируется в клетках ретикуломакрофагальной системы, локализованных в костном мозге, селезёнке, лимфатических узлах и печени. Процесс начинается с окислительного расщепления порфиринового кольца гема под действием гем-оксигеназы, что приводит к формированию биливердина.
Последующее восстановление биливердина ферментом биливердинредуктазой завершает первичную стадию образования билирубина[4]. Гем-оксигеназа существует в двух изоформах: конститутивной (HO-2) и индуцибельной (HO-1), которая активируется при стрессовых условиях.
Суточная продукция билирубина у взрослого человека составляет приблизительно 250—300 мг, при этом около 85 % образуется из гемоглобина стареющих эритроцитов, а оставшаяся часть — из других гем-содержащих белков и неэффективного эритропоэза.
Печёночные превращения и конъюгация
Транспорт билирубина к печени осуществляется в комплексе с альбумином плазмы крови, поскольку неконъюгированная форма характеризуется гидрофобностью. В гепатоцитах происходит ключевая реакция конъюгации с глюкуроновой кислотой при участии фермента УДФ-глюкуронилтрансферазы.
Количественное распределение фракций в крови демонстрирует преобладание непрямого билирубина (96 %), тогда как конъюгированные формы составляют лишь 4 % от общего содержания[5]. Концентрация прямого билирубина в сыворотке крови в норме составляет 1,7-8,5 мкмоль/л.
Процесс конъюгации происходит в два этапа: сначала образуется моноглюкуронид билирубина, затем — диглюкуронид. Диглюкуронидная форма составляет основную часть конъюгированного билирубина и обладает наибольшей растворимостью в воде.
Кишечный метаболизм и выведение
В тонкой кишке конъюгированный билирубин подвергается деконъюгации и восстановлению до уробилиногена под действием специализированного микробного фермента билирубинредуктазы[6]. Дальнейшие превращения в толстой кишке приводят к образованию стеркобилиногена, который окисляется до стеркобилина, обеспечивающего характерную коричневую окраску фекалий[7].
Энтерогепатическая циркуляция обеспечивает реабсорбцию около 5 % стеркобилиногена в системный кровоток с последующим выведением через почки.
Кишечная микрофлора играет критическую роль в метаболизме билирубина. У новорождённых недостаточная колонизация кишечника бактериями может приводить к обратному всасыванию неизменённого билирубина, что способствует развитию физиологической желтухи.
Защитные функции
Антиоксидантная защита
Фундаментальная роль билирубина в клеточной защите определяется его мощными антиоксидантными свойствами[8]. Циклические превращения между билирубином и биливердином создают эффективную систему нейтрализации активных форм кислорода.
Экспериментальные исследования на животных моделях демонстрируют, что элиминация билирубина приводит к развитию эндогенного оксидативного стресса, подчёркивая критическую важность данного соединения для поддержания клеточного гомеостаза.
Антиоксидантная активность билирубина превосходит таковую у витамина E и сопоставима с активностью глутатиона. Механизм действия включает прямое связывание пероксидных радикалов и предотвращение перекисного окисления липидов мембран.
Защита нервной системы
Особое значение антиоксидантной активности билирубина проявляется в нервной ткани, где он предотвращает эксайтотоксичность и нейрональную гибель путём улавливания супероксидных радикалов при N-метил-D-аспартатной нейротрансмиссии[9].
Способность билирубина проникать через гемато-энцефалический барьер при концентрациях выше 20-25 мг/100 мл может приводить как к токсическим эффектам, так и к реализации защитных функций в зависимости от физиологического контекста.
Нейропротективное действие билирубина особенно важно при ишемических повреждениях мозга, где локальное повышение его концентрации может ограничивать зону некроза и способствовать восстановлению нервной ткани.
Патологические состояния и клинические проявления
Классификация гипербилирубинемических состояний
Клиническая систематизация нарушений билирубинового обмена основывается на этиологическом принципе с выделением догеченочных, печёночных и послепеченочных причин[10]. Догеченочные факторы преимущественно связаны с усиленным гемолизом эритроцитов, тогда как печёночные нарушения включают наследственные ферментопатии, воспалительные процессы и токсические поражения.
Послепеченочная обструкция жёлчевыводящих путей характеризуется накоплением конъюгированных форм билирубина. Генетический синдром Жильбера, встречающийся у 5 % популяции, представляет наиболее распространённую форму наследственной гипербилирубинемии.
Дифференциальная диагностика основывается на определении соотношения фракций билирубина в крови. Преобладание непрямого билирубина характерно для гемолитических состояний, тогда как повышение прямой фракции указывает на печёночно-жёлчную патологию.
Изменение цвета тканей
Динамика изменения окраски кровоподтёков отражает последовательные этапы метаболизма гемоглобина in vivo[5]:
- Первоначальный багровый или багрово-синюшный оттенок гема сохраняется 1-4 суток.
- Зелёные пигменты (вердоглобин и биливердин) проявляются на протяжении 4-8 дней.
- Смешанные оттенки наблюдаются до 9-12 суток.
- Характерная жёлто-серая окраска, обусловленная накоплением билирубина, формируется на 12-16 день после травмы.
Данная цветовая эволюция используется в судебной медицине для определения давности травматических повреждений. Скорость изменения окраски может варьировать в зависимости от возраста пациента, состояния кровообращения и локализации гематомы.
Диагностика
Качественные реакции
Классическая проба Гаррисона, основанная на окислении билирубина до биливердина реактивом Фуше, характеризуется высокой чувствительностью 0,5-1,7 мг/100 мл[11]. Данный метод был унифицирован в советской лабораторной практике благодаря надёжности и воспроизводимости результатов.
Современные колориметрические подходы используют диазореакцию с образованием азобилирубина, интенсивность окрашивания которого пропорциональна концентрации исследуемого вещества. Метод Ван ден Берга остаётся основным принципом определения билирубина в клинических лабораториях. Различие во времени реакции позволяет дифференцировать прямой и непрямой билирубин: прямой реагирует немедленно, тогда как для непрямого требуется добавление ускорителей реакции.
Современные методы
Инновационная технология Vitros BuBc обеспечивает быстрое определение фракций билирубина у новорождённых, требуя лишь 70 мкл образца крови и 10 минут времени анализа[11]. Метод основан на многослойном разделении на полиэстеровой подложке, что позволяет дифференцировать различные формы билирубина с высокой точностью.
Фармакокинетические характеристики различных фракций существенно различаются: полужизнь свободного билирубина составляет 2-4 часа, тогда как дельта-билирубин, ковалентно связанный с альбумином, сохраняется в циркуляции 2-3 недели.
Современные анализаторы позволяют проводить неинвазивные измерения концентрации билирубина через кожу с использованием транскутанных билирубинометров, что особенно важно при мониторинге новорождённых.
Референтные значения и интерпретация
Нормальные концентрации билирубина в крови взрослых характеризуются чёткими диапазонами[12]:
- прямой билирубин: 0-0,3 мг/дл;
- общий билирубин: 0,1-1,2 мг/дл.
В системе СИ соответствующие значения составляют менее 21 мкмоль/л для общего и 1,0-5,1 мкмоль/л для прямого билирубина. Присутствие билирубина в моче здоровых людей в норме не детектируется, поскольку неконъюгированные формы не проходят почечный фильтр.
Интерпретация результатов должна учитывать возрастные особенности, время суток и условия забора материала. У новорождённых физиологическое повышение билирубина может достигать 200—250 мкмоль/л без признаков патологии.
Эволюция и распространение
Традиционное представление о билирубине как исключительно животном пигменте было пересмотрено после обнаружения данного соединения в растительных тканях Strelitzia nicolai[13]. Это открытие расширило понимание эволюционного распространения тетрапиррольных структур и поставило вопросы о функциональной роли билирубина в растительном метаболизме.
Филогенетические связи между животными и растительными тетрапиррольными пигментами указывают на древность данных биохимических путей.
Присутствие билирубина в растениях предполагает существование альтернативных путей его синтеза, не связанных с катаболизмом гемоглобина. Возможно, растительный билирубин выполняет защитные функции против фотоокислительного стресса или участвует в регуляции светозависимых процессов.
История изучения
Научное изучение билирубина берёт начало в 1827 году с работ М. Луи Жака Тенара, исследовавшего жёлчный тракт слона в парижском зоопарке[14]. Систематическая номенклатура была заложена в 1864 году Штёделером, который кристаллизовал билирубин из жёлчных камней крупного рогатого скота.
Идентичность билирубина и гематоидина была окончательно установлена Фишером и Штейнмецем в 1923 году с использованием аналитической кристаллографии. Современный этап исследований начался с открытия гем-оксигеназы Руди Шмидом и Тенхуненом в 1968 году, что позволило расшифровать молекулярные механизмы биосинтеза билирубина.
Важным этапом стало понимание роли билирубина как антиоксиданта в 1980-х годах, что кардинально изменило представления о его биологической значимости. Ранее билирубин рассматривался исключительно как токсичный продукт распада, однако современные исследования показали его критическую важность для защиты клеток от оксидативного стресса.
Литература
- Антина Е. В., Румянцев Е. В. Химия билирубина и его аналогов. — М.: КРАСАНД, 2009.
- Kuntz E. Hepatology: Textbook and Atlas. — Heidelberg: Springer, 2008.
Примечания
- ↑ Серов В. В., Пальцев М. А. Патологическая анатомия. Курс лекций. — М.: Медицина, 1998. — С. 59.
- ↑ 2,0 2,1 Никольский Б. П. Справочник химика. — Рипол Классик, 2014.
- ↑ Лошкова Е. В. и др. Синдром Жильбера как модель изучения эффектов билирубина // Экспериментальная и клиническая гастроэнтерология. — 2022. — Т. №. 10 (206). — С. 126–141.
- ↑ Таболин В. А. Билирубин // Большая медицинская энциклопедия. — 3-е изд. — М.: Советская энциклопедия, 1976. — Т. 3.
- ↑ 5,0 5,1 Hall B., Levy S., Dufault-Thompson K. BilR is a gut microbial enzyme that reduces bilirubin to urobilinogen // Nature Microbiology. — 2024. — Т. 9, no. 1. — С. 173–184.
- ↑ Березов Т. Т., Коровкин Б. Ф. Биологическая химия: Учебник. — М.: Медицина, 2004. — С. 704.
- ↑ Березов Т. Т., Коровкин Б. Ф. Биологическая химия: Учебник. — М.: Медицина, 2004. — С. 704.
- ↑ Baranano D. E., Rao M., Ferris C. D., Snyder S. H. Biliverdin reductase: A major physiologic cytoprotectant // Proceedings of the National Academy of Sciences of the United States of America. — 2002. — Т. 99, no. 25. — С. 16093–16098.
- ↑ Vasavda C., Kothari R., Malla A. P. Bilirubin Links Heme Metabolism to Neuroprotection by Scavenging Superoxide // Cell Chemical Biology. — 2019. — Т. 26, no. 10. — С. 1450–1460.
- ↑ Roche S. P., Kobos R. Jaundice in the Adult Patient // American Family Physician. — 2004. — Т. 69, no. 2. — С. 299–304.
- ↑ 11,0 11,1 Poventud‐Fuentes I. et al. Interference of eltrombopag with bilirubin measurements on the Vitros 5600 analyzer //Journal of Clinical Laboratory Analysis. — 2021. — Т. 35. — №. 8.
- ↑ Щербинина М. Б. Низкий уровень билирубина крови: возможное диагностическое и прогностическое значение // Клиническая медицина. — 2007. — Т. 85. — №. 10. — С. 10–14.
- ↑ Комаров Ф. И., Коровкин Б. Ф. Биохимические исследования в клинике. — Л.: Медицина, 1981. — С. 218.
- ↑ Pirone C., Quirke J. M. E., Priestap H. A., Lee D. W. Animal Pigment Bilirubin Discovered in Plants // Journal of the American Chemical Society. — 2009. — Т. 131, no. 8. — С. 2830.