Ноотропы
Ноотро́пы (греч. νόος — разум и греч. τροπ — поворот, изменение) — гетерогенная группа фармакологических агентов, декларируемая способность которых заключается в модуляции высших психических функций человека. Концептуальное оформление данной категории веществ произошло в 1972 году[1], когда бельгийский исследователь впервые систематизировал специфические нейротропные эффекты, не укладывающиеся в традиционные рамки психофармакологии.
В современной медицинской практике ноотропы занимают особое положение, характеризующееся значительными географическими различиями в признании и применении. Широкое использование данных препаратов в странах постсоветского пространства контрастирует с их практически полным отсутствием в клинических протоколах развитых западных государств. Эта дихотомия отражает фундаментальные разногласия в оценке доказательной базы эффективности и создаёт уникальную ситуацию в мировой фармакологии, где целый класс препаратов имеет диаметрально противоположный статус в различных регулятивных системах.
Основы концепции и терминология
Развитие понятия
Лингвистическая конструкция термина отражает базовую философию воздействия на познавательные процессы. Композитная структура слова указывает на направленное изменение ментальных функций.
Это изначально предполагало качественно новый подход к фармакологической коррекции когнитивных нарушений. Введение специализированной номенклатуры было обусловлено необходимостью категоризации эффектов пирацетама, не соответствовавших известным психотропным паттернам[1].
Международная терминология
В англоязычной научной среде укоренилось альтернативное обозначение данной группы веществ как «интеллектуальных фармакологических средств»[2]. Наряду с ним применяются и другие дескрипции.
В научных публикациях встречаются термины «нейрометаболические стимуляторы», «когнитивные модуляторы» и «усилители познавательной деятельности». Подобная терминологическая множественность отражает концептуальную неопределённость самой области исследований.
Требования к препаратам
Первоначальные требования к ноотропным препаратам включали пять основных характеристик[2]:
- улучшение процессов обучения и памяти;
- повышение резистентности к факторам, нарушающим приобретённые навыки;
- защита мозга от физических и химических повреждений;
- усиление эффективности корковых контрольных механизмов;
- отсутствие типичной фармакологии психотропных средств с минимальными побочными эффектами.
Однако современный анализ показывает, что большинство веществ, позиционируемых как ноотропы, не соответствуют этим изначальным критериям.
История изучения
Начало исследований
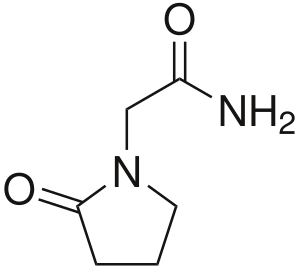
Фундаментальный прорыв в данной области произошёл в 1964 году, когда бельгийские фармакологи синтезировали пирацетам — первое соединение нового класса[3]. Этот препарат, впоследствии коммерциализированный под торговым наименованием «ноотропил», продемонстрировал необычный спектр нейрофармакологической активности.
Последующая теоретическая работа привела к формулированию критериев, которым должны соответствовать препараты новой категории. А именно: улучшение процессов обучения и запоминания, повышение резистентности мозговых структур к повреждающим воздействиям, отсутствие типичных побочных эффектов психостимуляторов.
Современные исследования и изменение взглядов
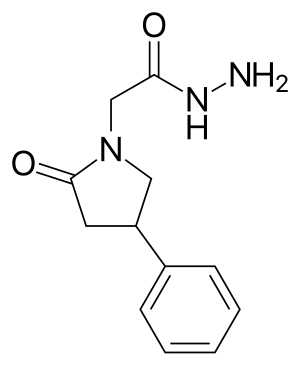
Интенсивное развитие химического синтеза привело к созданию более десяти оригинальных соединений пирролидинового ряда, получивших собирательное название «рацетамы». Среди них выделяются оксирацетам, анирацетам, этирацетам, прамирацетам и другие структурные аналоги. Однако современные реалии фармацевтического рынка демонстрируют серьёзные проблемы с качеством коммерческих препаратов[4].
Развитие области ноотропов характеризуется постепенным смещением от первоначального энтузиазма к более критическому анализу. Если в начальный период исследований превалировала оптимистическая оценка потенциала новых веществ, то накопление клинических данных выявило существенные ограничения концепции. Современная научная парадигма требует строгих доказательств эффективности, что создаёт значительные препятствия для признания ноотропных эффектов[4].
Механизмы действия
- Молекулярные мишени воздействия
Современная нейрофармакология рассматривает несколько ключевых путей реализации предполагаемых эффектов ноотропов. Активация аденилатциклазы приводит к повышению внутриклеточной концентрации циклического аденозинмонофосфата, что инициирует каскад биохимических реакций. Установлено, что модуляция серотонинергической передачи через цАМФ-зависимые механизмы способствует ускоренному высвобождению глутамата из пресинаптических терминалей[5].
- Нейромедиаторные системы
Предполагаемые терапевтические эффекты реализуются через взаимодействие с различными нейротрансмиттерными системами мозга. Холинергические механизмы особенно выражены у фенотропила, тогда как глутаматергические пути активируются через NMDA-рецепторы при применении мемантина и глицина. Рацетамы демонстрируют свойства положительных аллостерических модуляторов AMPA-рецепторов, хотя полное понимание их молекулярных механизмов остаётся неполным[5].
- Энергетический метаболизм мозга
Активированная аденилатциклаза поддерживает стабильность выработки аденозинтрифосфата без участия кислорода, что теоретически обеспечивает нейропротективный эффект в условиях гипоксии. Этот механизм переводит метаболизм мозга в режим оптимального сохранения энергетических ресурсов при неблагоприятных условиях. Однако клиническая значимость подобных биохимических изменений остаётся предметом дискуссий[5].
- Нейропластичность и синаптическая передача
Декларируемое улучшение кортико-субкортикального контроля и информационного обмена в мозге составляет основу теоретических представлений о механизмах действия ноотропов. Предполагается, что позитивное воздействие на формирование и воспроизведение памятного следа обеспечивает улучшение восприятия, внимания, мышления и способности к обучению. Тем не менее, переход от молекулярных эффектов к клинически значимым изменениям когнитивных функций не получил убедительного обоснования[5].
Доказательная база эффективности
Критический анализ клинических данных
Фундаментальная проблема ноотропной фармакологии заключается в отсутствии убедительных доказательств терапевтической эффективности[6]. Регулятивные органы развитых стран не признают клиническую значимость этих препаратов, что отражается в их отсутствии в официальных фармакопеях. Количественный анализ исследовательской базы демонстрирует впечатляющие цифры: пирацетам изучался в 333 клинических испытаниях начиная с 1972 года, циннаризин — в 137 исследованиях с 1966 года, церебролизин — в 53 работах с 1976 года.
- Официальные предупреждения
Надзорные органы здравоохранения выражают серьёзную обеспокоенность относительно маркетинговых практик производителей ноотропных добавок[7]. Выявлены многочисленные случаи недобросовестной рекламы, содержащей недоказанные утверждения о терапевтической эффективности. Параллельно документируются нарушения в составе коммерческих препаратов, включая присутствие неразрешённых субстанций.
- Оценка доказательств
Современная доказательная медицина использует четыре основных уровня убедительности научных данных. «Золотой стандарт» (уровень А) представлен результатами качественных рандомизированных контролируемых исследований и систематических обзоров. Уровень D (или E) основывается исключительно на мнении экспертов при отсутствии контролируемых клинических исследований. Большинство ноотропных препаратов имеют доказательную базу не выше уровня С, а многие не достигают даже этого показателя[7].
- Позиция профессиональных медицинских организаций
Американская медицинская ассоциация в 2016 году официально рекомендовала воздерживаться от назначения ноотропов здоровым людям. Данное решение основывалось на вариабельности когнитивных эффектов между индивидуумами, их дозозависимости и в целом ограниченной или умеренной выраженности. Кокрейновская библиотека, представляющая независимые сводные данные об эффективности медицинских вмешательств, не содержит убедительных доказательств пользы большинства ноотропных препаратов[7].
- Систематические обзоры и мета-анализы
Проведённые систематические обзоры результатов клинических исследований пирацетама не подтвердили его эффективность, что требует дальнейших исследований. Винпоцетин, несмотря на 27 клинических испытаний начиная с 1985 года, имеет все показания к применению со степенью доказанности не выше «С», а большинство — на уровне «D». Для гопантеновой кислоты доказательные сведения об эффективности и безопасности в авторитетных базах данных отсутствуют полностью[7].
Классификация препаратов
Производные пирролидона
Основную группу классических ноотропов составляют структурные аналоги пирацетама. Эти соединения не имеют самостоятельного статуса в международных классификационных системах и формально относятся к психостимуляторам с присвоением кода N06ВХ.
Производные диафенилпирролидона, представленные фенотропилом, демонстрируют расширенный спектр фармакологической активности[6].
Биологически активные соединения
Нейропептидная группа включает как природные, так и синтетические аналоги регуляторных пептидов: ноопепт, семакс, селанк. Производные гамма-аминомасляной кислоты (пикамилон, фенибут, гопантеновая кислота) теоретически модулируют ГАМКергическую нейротрансмиссию.
Витаминоподобные соединения, такие как идебенон, а также полипептидные комплексы (кортексин, церебролизин) расширяют номенклатуру доступных препаратов[6].
Центральные стимуляторы с когнитивными эффектами
Систематические обзоры и мета-анализы показывают, что низкие дозы определённых стимуляторов центральной нервной системы могут улучшать когнитивные функции у здоровых людей[8]. Особенно это касается препаратов, действующих как прямые или непрямые агонисты дофаминовых D1-рецепторов или адренорецепторов A2. Амфетамин в низких дозах улучшает тормозной контроль, эпизодическую память, рабочую память и аспекты внимания[9].
Кофеин остаётся наиболее широко потребляемым ноотропным веществом в мире. В 2008 году стимуляторы, включая кофеин, были наиболее часто используемыми ноотропными агентами. Мета-анализы демонстрируют увеличение бдительности и улучшение показателей внимания при его применении. Модафинил может улучшать бдительность, особенно у людей с недостатком сна, и способствовать улучшению рассуждения и решения проблем.
Холинергические соединения и предшественники ацетилхолина
Некоторые предполагаемые ноотропные вещества представляют собой соединения и аналоги холина — предшественника ацетилхолина и фосфатидилхолина. Холина битартрат, согласно мета-анализу, неэффективен для улучшения любых показателей когнитивной деятельности.
В противоположность этому, цитиколин может быть эффективен для улучшения памяти и обучения у пожилых людей с лёгким когнитивным снижением и у людей, восстанавливающихся после инсульта[6].
Растительные экстракты и нутрицевтики
Мета-анализ 2017 года не показал значительного улучшения когнитивной функции от применения Centella asiatica. Экстракт листьев Ginkgo biloba продаётся в форме диетических добавок с утверждениями о способности улучшать когнитивные функции, хотя высококачественные доказательства таких эффектов на память или внимание у здоровых людей отсутствуют. Кокрейновский обзор Panax ginseng выявил возможное улучшение некоторых аспектов когнитивной функции, поведения и качества жизни, но отсутствие убедительных доказательств когнитивно-улучшающего эффекта у здоровых участников.
Фолат, омега-3 жирные кислоты (DHA и EPA), витамины B12, B6 и E не демонстрируют когнитивно-улучшающих эффектов у людей среднего и пожилого возраста без соответствующих дефицитов. Два кокрейновских обзора использования омега-3 жирных кислот при СДВГ и расстройствах обучения пришли к выводу об ограниченных доказательствах терапевтических преимуществ[6].
Клиническое применение
- Неврологические показания
В странах с менее строгим фармацевтическим регулированием ноотропы широко применяются при различных патологических состояниях центральной нервной системы. Спектр использования охватывает деменции различной этиологии, хроническую цереброваскулярную недостаточность, психоорганический синдром. Дополнительными показаниями служат последствия нарушений мозгового кровообращения, черепно-мозговых травм, интоксикаций и нейроинфекций[1].
- Педиатрическая практика
Детская неврология активно использует ноотропные препараты при задержках психического и речевого развития, умственной отсталости, последствиях перинатальных поражений центральной нервной системы. Синдром дефицита внимания и детский церебральный паралич также рассматриваются как потенциальные области применения. Некоторые препараты используются для коррекции заикания, гиперкинезов, расстройств мочеиспускания и нарушений сна[1].
- Специализированные применения
Отдельные ноотропы находят применение для коррекции нейролептического синдрома (деанола ацеглумат, пиритинол, пантогам, гопантеновая кислота). В офтальмологии в составе комплексной терапии применяются никотиноил-ГАМК при открытоугольной глаукоме, сосудистых заболеваниях сетчатки и жёлтого пятна. Некоторые препараты используются для профилактики укачивания и лечения мигрени[1].
- Противоречия в профилактике инсульта
Эффективность ноотропов для профилактики и лечения инсультов подвергается обоснованным сомнениям. Их применение не подтверждено методами доказательной медицины и не входит в стандарты профилактики и лечения острых нарушений мозгового кровообращения. Данное обстоятельство создаёт этические проблемы в клинической практике, особенно учитывая серьёзность цереброваскулярной патологии[10].
Безопасность и побочные эффекты
Известные нежелательные реакции
Несмотря на репутацию относительно безопасных средств, ноотропы способны вызывать серьёзные осложнения. Особую опасность представляет развитие лекарственного паркинсонизма при использовании циннаризина, особенно в гериатрической популяции[10]. Наиболее распространёнными побочными эффектами являются нарушения сна, тревожность и повышенная раздражительность.
Рацетамы и структурно родственные пирацетаму соединения характеризуются относительно низкой токсичностью и редкими серьёзными побочными эффектами. Тем не менее, доказательства их способности улучшать познавательные функции у людей без когнитивных нарушений практически отсутствуют. Это создаёт парадоксальную ситуацию, когда препараты с хорошим профилем безопасности не демонстрируют клинически значимой эффективности.
Дозозависимые эффекты и нарушения когнитивных функций
Важным аспектом безопасности является дозозависимость терапевтических и нежелательных эффектов. Относительно высокие дозы стимуляторов могут вызывать когнитивные нарушения, противоположные желаемому эффекту.
Метилфенидат в дозах выше оптимальных проявляет нецелевые эффекты, которые ухудшают способность к обучению. Подобная закономерность подчёркивает важность точного дозирования и индивидуального подбора терапии[10].
Особые предостережения
Применение ноотропных средств у пациентов с тяжёлыми психическими расстройствами может спровоцировать обострение основного заболевания. Лечение инсомнии данной группой препаратов оправдано только при дефицитарном генезе нарушений сна. Во время терапии рекомендуется соблюдать осторожность при управлении транспортными средствами и работе с потенциально опасными механизмами[10].
Особую осторожность следует проявлять при назначении ноотропов пациентам с биполярным аффективным расстройством и шизофренией. У данной категории больных активация познавательных процессов может сопровождаться дестабилизацией психического состояния и требует тщательного мониторинга клинического статуса.
Долгосрочные эффекты и взаимодействия
Длительная безопасность многих ноотропных соединений остаётся недостаточно изученной. Основная обеспокоенность связана с возможностью развития психологической зависимости при длительном применении. Комбинированная терапия создаёт возможности не только для потенцирования положительных эффектов, но и для усиления нежелательных явлений, что требует особой осторожности при назначении нескольких препаратов одновременно[10].
Отсутствие долгосрочных данных безопасности является типичным для многих ноотропных соединений. Это обстоятельство создаёт дополнительные риски при длительном применении, особенно у молодых пациентов. Потенциал развития толерантности и необходимость увеличения доз остаются малоизученными аспектами долгосрочной терапии.
Проблемы качества и фальсификации
Современный рынок ноотропных добавок характеризуется серьёзными проблемами контроля качества. Выявлены многочисленные случаи несоответствия фактического состава заявленному на этикетке, присутствие неразрешённых субстанций и сокрытие активных фармацевтических ингредиентов. Подобные нарушения создают непредсказуемые риски для потребителей и затрудняют оценку истинного профиля безопасности препаратов[10].
Некоторые диетические добавки могут содержать скрытые лекарственные вещества, что создаёт риск непреднамеренного приёма неразрешённых препаратов с неизвестным профилем безопасности. Данная проблема особенно актуальна для продуктов, приобретаемых через интернет без надлежащего фармацевтического контроля.
Литература
- Battleday R. M., Brem A. K. Modafinil for cognitive neuroenhancement in healthy non-sleep-deprived subjects: A systematic review // European Neuropsychopharmacology. — 2015.
- Forbes S. C., Holroyd-Leduc J. M., Poulin M. J., Hogan D. B. Effect of Nutrients, Dietary Supplements and Vitamins on Cognition: a Systematic Review and Meta-Analysis of Randomized Controlled Trials // Canadian Geriatrics Journal. — 2015.
- Geng J., Dong J., Ni H. Ginseng for cognition // The Cochrane Database of Systematic Reviews. — 2010.
- Laws K. R., Sweetnam H., Kondel T. K. Is Ginkgo biloba a cognitive enhancer in healthy individuals? A meta-analysis // Human Psychopharmacology. — 2012.
- Malykh A. G., Sadaie M. R. Piracetam and piracetam-like drugs: from basic science to novel clinical applications to CNS disorders // Drugs. — 2010.
Примечания
- ↑ 1,0 1,1 1,2 1,3 1,4 Giurgea C. «Pharmacology of integrative activity of the brain. Attempt at nootropic concept in psychopharmacology» // Actualites Pharmacologiques (in French). — 1972. — № 25. — С. 115–156. — PMID 4541214.
- ↑ 2,0 2,1 Smart Drugs and Should We Take Them Архивная копия от 19 ноября 2012 на Wayback Machine, 2009
- ↑ Dr. Corneliu E. Giurgea — The Father of Nootropics Архивная копия от 15 февраля 2018 на Wayback Machine.
- ↑ 4,0 4,1 Cohen PA, Zakharevich I, Gerona R. «Presence of Piracetam in Cognitive Enhancement Dietary Supplements»» // JAMA Internal Medicine. — 2020. — Март (№ 180). — С. 458–459. — doi:10.1001/jamainternmed.2019.5507. — PMID 31764936.
- ↑ 5,0 5,1 5,2 5,3 P. J. Bergold, J. D. Sweatt, I. Winicov, K. R. Weiss, E. R. Kandel. Protein synthesis during acquisition of long-term facilitation is needed for the persistent loss of regulatory subunits of the Aplysia cAMP-dependent protein kinase (англ.) // Proceedings of the National Academy of Sciences. — Vol. 87. — С. 3788–3791. — doi:10.1073/pnas.87.10.3788.
- ↑ 6,0 6,1 6,2 6,3 6,4 Комаровский Е. О. О лекарствах, которые «улучшают работу мозга», или Про ноотропные средства // Сайт «Доктор Комаровский». Архивировано 8 декабря 2021 года.
- ↑ 7,0 7,1 7,2 7,3 «FTC and FDA Send Warning Letters to Companies Selling Dietary Supplements Claiming to Treat Alzheimer’s Disease and Remediate or Cure Other Serious Illnesses Such as Parkinson’s, Heart Disease, and Cancer». US Food and Drug Administration, US Federal Trade Commission. February 11, 2019. Retrieved May 11, 2019.
- ↑ Spencer RC, Devilbiss DM, Berridge CW. «The cognition-enhancing effects of psychostimulants involve direct action in the prefrontal cortex» // Biological Psychiatry. — 2018. — Ноябрь (№ 77). — С. 940–950. — doi:10.1016/j.biopsych.2014.09.013. — PMID 25499957.
- ↑ Ilieva IP, Hook CJ, Farah MJ. «Prescription Stimulants' Effects on Healthy Inhibitory Control, Working Memory, and Episodic Memory: A Meta-analysis» (англ.) // Journal of Cognitive Neuroscience. — Июнь (№ 27). — С. 1069–1089. — doi:10.1162/jocn_a_00776. — PMID 25591060.
- ↑ 10,0 10,1 10,2 10,3 10,4 10,5 Marti-Masso J. F., Poza J. J. Cinnarizine-induced parkinsonism: ten years later // Movement Disorders. — 1998. — Т. 13. — С. 453–456.
Ссылки
- Лесиовская Е. Е., Марченко Н. В., Пивоварова А. С. Сравнительная характеристика лекарственных средств, стимулирующих ЦНС. Ноотропные препараты. / Фарминдекс, Практик № 4 2003.
- Лечение инсульта: ноотропы или доказательная медицина? (Перевод с англ. Корзун А. И.)
- Стивен Холл, Виагра для мозга — статья из журнала «В мире науки», декабрь 2003 № 12
- SMART DRUGS 2 THE NEXT GENERATION Ресурс по ноотропикам проекта Better Living Through Chemistry
- Васильева С. Ноотропы: работают ли полипептиды коры головного мозга скота?