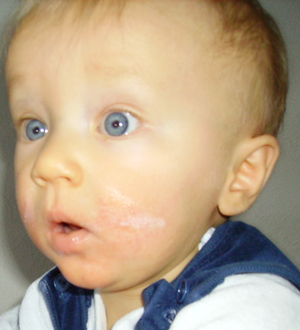
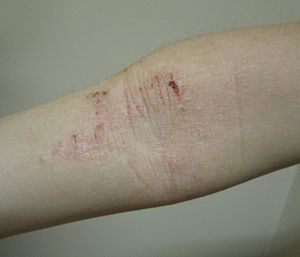
Атопический дерматит
Атопи́ческий дермати́т (АтД) представляет собой хроническое воспалительное заболевание кожных покровов[1]. Данное состояние характеризуется ранним дебютом, как правило, в детском возрасте, с возможностью персистирования или рецидивирования во взрослом периоде жизни. АтД не относится к контагиозным патологиям.
| Атопический дерматит | |
|---|---|
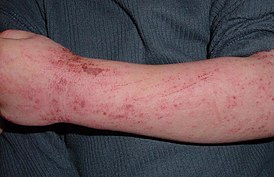 Атопический дерматит у ребёнка Атопический дерматит у ребёнка | |
| МКБ-10 | L20 |
| МКБ-9 | 691.8 |
| OMIM | 603165 |
| DiseasesDB | 4113 |
| eMedicine | emerg/130 derm/38 ped/2567 oph/479 |
Этиология
Этиология заболевания преимущественно связана с генетической предрасположенностью. Нередко АтД сопутствуют иные аллергические состояния, включая бронхиальную астму (БА), аллергический ринит (АР), пищевую аллергию (ПА). Также отмечается склонность к рецидивирующим кожным инфекциям[1].
Эпидемиология
Распространённость АтД в развитых странах — 10-20% популяции. Манифестация симптоматики АтД у детей фиксируется в 60% случаев к 6 месяцам, в 75% — до года, в 80-90% — до 7 лет[2].
На протяжении минувших десятилетий регистрируется существенный прирост заболеваемости АтД, усугубление его течения и исходов.
В XX веке была доказана взаимосвязь АтД, поллиноза и бронхиальной астмы — комплекс, обозначенный термином «атопическая триада».
Классификация
В 2001 году EAACI предложила заменить термин «атопический дерматит» на AEDS («САЭД — синдром атопической экземы/дерматита»), который подразделяется на[3]:
- неаллергический САЭД;
- аллергический САЭД:
— IgE-опосредованный САЭД;
— не IgE-опосредованный САЭД.
В России используется классификация согласно МКБ-10[3]:
- атопический дерматит:
- почесуха Бенье;
- другие атопические дерматиты:
- экзема (дерматит):
- сгибательная (если не относится к иным видам экзем или дерматитов);
- детская (острая или хроническая);
- эндогенная (аллергическая);
- нейродермит (нейродерматит):
- атопический (локализованный);
- диффузный;
- атопический дерматит неуточненный.
Клинические формы атопического дерматита в зависимости от возраста
В зависимости от возраста клинические формы АтД бывают[1]:
- Младенческая форма — наблюдается у детей от одного месяца до двух лет.
- Детская форма — характерна для возрастной группы от двух до двенадцати лет.
- Подростковая форма — диагностируется у лиц старше двенадцати лет.
Критерии диагностики атопического дерматита
Основные (обязательные) диагностические критерии[4]:
- Пруриго (зуд) даже при наличии минимальных кожных проявлений.
- Характерная морфология и локализация высыпаний (лицо, шея, подмышечные впадины, локтевые и подколенные ямки, паховая область, волосистая часть головы, области под мочками ушей и др.).
- Индивидуальный или семейный анамнез атопических заболеваний.
- Хроническое рецидивирующее течение.
Дополнительные диагностические критерии[4]:
- повышенный уровень общего и специфических IgE-антител;
- дебют заболевания в раннем детском возрасте (до 2 лет);
- гиперлинеарность ладоней и подошв;
- pityriasis alba (белесоватые пятна на коже лица, плечевого пояса);
- фолликулярный гиперкератоз на боковых поверхностях плеч, предплечий, локтей;
- шелушение, ксероз, ихтиоз;
- неспецифические дерматиты кистей и стоп;
- частые инфекционные поражения кожи (стафилококковой, грибковой, герпетической этиологии);
- белый дермографизм;
- зуд при гипергидрозе;
- складки на передней поверхности шеи;
- периорбитальная пигментация («аллергическое сияние»);
- шелушение, эритема, зуд после водных процедур (у детей до 2 лет).
Диагноз АтД устанавливается при наличии трёх основных и не менее трёх дополнительных критериев[5]
Патогенез
АтД представляет собой мультифакторное заболевание, в этиологии которого участвуют генетическая предрасположенность, средовые факторы и иммунологические нарушения. Патогенез АтД характеризуется хроническим воспалением 2 типа (Т2-воспаление). У почти 50% пациентов с АтД средней и тяжёлой степени выявляется как минимум одна мутация гена филаггрина[6].
В современной науке существуют две концепции, объясняющие патофизиологические механизмы АтД: «снаружи-внутрь» (нарушение барьерной функции кожи) и «наружу-изнутри» (иммунная дисрегуляция).
Цитокины, ассоциированные с воспалением 2-го типа (Т2-воспаление), инициируют каскад сигнальных и эффекторных механизмов, приводящих к патологическим изменениям кожного покрова при атопическом дерматите (АтД)[9]. Центральное место в патогенезе АтД занимают интерлейкины 4 и 13 (ИЛ-4 и ИЛ-13). Эти медиаторы оказывают комплексное воздействие на иммунную систему и структуру кожи.
На иммунологическом уровне ИЛ-4 и ИЛ-13 способствуют нарушению регуляции иммунного ответа. Они стимулируют трансформацию наивных Т-лимфоцитов-хелперов в Т-хелперы 2-го типа (Th2) и индуцируют переключение В-лимфоцитов на продукцию иммуноглобулина Е (IgE).
На тканевом уровне эти интерлейкины вызывают ряд структурных изменений в коже:
- гиперплазию эпидермиса;
- развитие фиброза;
- подавление синтеза антимикробных пептидов;
- снижение продукции барьерных белков, включая филаггрин;
- нарушение липидного состава кожи, в частности, уменьшение содержания церамидов.
Совокупность этих процессов приводит к формированию характерной для АтД клинической картины поражения кожных покровов.
Лечение
Уход за кожей
Увлажняющие (смягчающие) средства (эмоленты)
Базовой рекомендацией для всех пациентов с атопическим дерматитом (АтД), независимо от тяжести заболевания, является топическое применение эмолентов — средств, обладающих увлажняющими и смягчающими свойствами[6].
Эмоленты представлены широким спектром лекарственных форм: лосьоны, кремы, мази, а также специализированные моющие средства и препараты для ванн. Подбор конкретного средства и его формы осуществляется на индивидуальной основе, учитывая ряд факторов: личные предпочтения пациента, специфические особенности кожного покрова, сезонность и климатические условия.
Протокол применения эмолентов предусматривает их систематическое и обильное нанесение не реже 3-4 раз в день. Эта процедура выполняется как самостоятельно, так и после гигиенических водных процедур. Некоторые исследования указывают на преимущество нанесения эмолентов на сухую кожу, без предварительного увлажнения.
Оптимальный терапевтический эффект достигается при регулярном использовании эмолентов в различных формах: кремы, мази, масла для ванн и специальные очищающие средства, заменяющие обычное мыло. Важным требованием к составу этих препаратов является отсутствие ароматизаторов, красителей и консервантов.
Сезонный подход к выбору эмолентов предполагает использование более жирных препаратов на мазевой основе в холодное время года, в то время как летом предпочтение отдаётся кремам и гелям с повышенным содержанием воды. Следует отметить, что лосьоны, характеризующиеся высоким содержанием легко испаряющейся воды, не рекомендованы пациентам с выраженным ксерозом кожи[6].
Эмоленты:
- Являются компонентом современного стандарта терапии АтД и необходимы в период ремиссии.
- Восстанавливают целостность водно-липидного и рогового слоёв эпидермиса, улучшают барьерную функцию кожи, используются для контроля симптомов заболевания.
- Применяются для предотвращения раздражающего действия ирритантов и детергентов, а также профилактически перед определёнными видами деятельности.
- Наносятся регулярно, не менее 2 раз в день, при необходимости до 5-7 раз в сутки; требуемый объём: для взрослых — до 600 г в неделю, для детей — до 250 г в неделю при обострениях[7].
- Особенно важно применение на руках и лице.
- Грудным детям рекомендуется наносить на руки и щёки до приёма пищи.
- При использовании других средств (кортикостероиды, ингибиторы кальциневрина) их следует наносить не раньше чем через 30 минут после эмолентов.
- Важен не только подбор эмолентов, но и кратность, количество и техника нанесения.
Профилактика обострений АтД
Нарушение целостности эпидермального барьера является одним из ключевых патогенетических механизмов развития АтД. Это приводит к повышенной потере влаги, усилению сухости кожи, что провоцирует зуд и расчёсывание. Последнее, в свою очередь, вызывает повторное повреждение эпидермиса, формируя порочный круг[7].
Рекомендации по созданию адекватного микроклимата:
- Поддержание оптимальной температуры воздуха (20-22°С в дневное время, 18-20°С ночью).
- Обеспечение относительной влажности в помещении 40-60% (оптимально 50-60%).
Рекомендации по подбору одежды[7]:
- Использование одежды из натуральных материалов (хлопок, лён, фланель, бамбук) с длинными рукавами и штанинами.
- Ношение свободной, неприлегающей одежды, исключающей натирание.
- Минимизация контакта кожи с верхней одеждой, синтетикой, красителями.
- Исключение закрытой облегающей тесной грубой одежды, особенно из шерсти, синтетики, меха животных, флиса, полиэстера.
Рекомендации по уходу за одеждой и бытовой гигиене:
- Исключение использования раздражающих веществ при стирке: стиральных порошков, сильных моющих средств, растворителей, бензина.
- Отказ от применения клеев, лаков, красок, средств для чистки мебели, полов, ковров.
Уход за ногтями:
- Поддержание коротко остриженных ногтей для предупреждения повреждения кожи при расчёсывании.
- Соблюдение чистоты ногтей для профилактики инфицирования расчёсов.
Рекомендации по образу жизни:
- Избегание пассивного курения.
Правила пребывания на солнце[7]:
- Умеренное пребывание на солнце без особых ограничений.
- Ограничение времени нахождения на солнце в период с 10 до 17 часов.
- Использование солнцезащитных средств при выходе на улицу в жаркое время суток.
- Ношение одежды, закрывающей руки и ноги, использование шляп с полями.
- Нанесение солнцезащитного крема за 30 минут до выхода и повторно каждые 2 часа.
- Рекомендация летнего отдыха в горах или на море.
Рекомендации по занятиям спортом[7]:
- Спортивные занятия не запрещены.
- Предпочтительны виды спорта с минимальным потоотделением.
- При провокации обострений потоотделением рекомендуется постепенная адаптация к нагрузкам.
- Ограничение участия в подвижных спортивных состязаниях.
- При необходимости участия в активных видах спорта следует применять тактику, аналогичную посещению бассейна: принять душ, нанести эмолент.
Рекомендации по посещению бассейна[7]:
- Переносимость индивидуальна (аналогично купанию в море).
- Предпочтительно использование бассейнов с нехлорированной водой.
- Для минимизации негативного воздействия рекомендуется после сеанса принять душ с применением мягких очищающих средств.
- После водных процедур необходимо нанесение увлажняющих и смягчающих препаратов.
Топическая (местная, наружная) терапия[6]
При лечении АтД лёгкой степени тяжести рекомендуется использование низко- и умеренно-активных топических глюкокортикоидов. В случаях среднетяжёлого и тяжёлого течения АтД целесообразно применение активных и высокоактивных топических глюкокортикоидов в минимальных эффективных дозировках, а также использование топических ингибиторов кальциневрина[6]
Для купирования обострений АтД возможно сочетанное применение наружных лекарственных средств и эмолентов с использованием техники влажных повязок.
«Проактивная» терапия АтД[7]
В традиционной терапии обострений АтД использовалась местная противовоспалительная терапия, включающая топические глюкокортикостероиды (ТГКС) и топические ингибиторы кальциневрина (ТИК). После купирования обострения применение препаратов прекращалось до следующего эпизода. Данный подход назывался «реактивным» лечением.
В последнее десятилетие разрабатывались методы снижения частоты обострений АтД. Была предложена «проактивная» тактика лечения, предполагающая нанесение ТГКС или ТИК в низких дозах на участки кожи, наиболее подверженные обострениям (локтевые сгибы, подколенные ямки), в сочетании с ежедневным использованием эмолентов.
Клинические исследования проводились с применением:
- ТГКС: метилпреднизолона ацепонат и флутиказона пропионат (длительностью до 16 недель);
- ТИК: такролимус (длительностью до 52 недель).
Клинический опыт и данные исследований показывают эффективность такролимуса и ГКС II и III классов для «проактивного» лечения, в то время как пимекролимус и ГКС I класса демонстрируют меньшую эффективность.
Физиотерапевтическое лечение (фототерапия)[6]
Фототерапия рекомендуется для лечения пациентов с атопическим дерматитом среднетяжёлой и тяжёлой степени[6]. Ультрафиолетовое излучение, применяемое в терапии АтД, обладает противовоспалительным действием на кожу и потенциальным антибактериальным эффектом. Применение различных видов фототерапии может иметь ограничения для определённых групп пациентов, в частности, для детей младше 5 лет.
Системная терапия атопического дерматита[6]
Биологическая терапия
Биологическая терапия АтД основана на применении генно-инженерных биологических препаратов — моноклональных антител, селективно блокирующих патогенетические механизмы заболевания. Данный вид терапии характеризуется высокой эффективностью и благоприятным профилем безопасности, не требующим регулярного мониторинга.
Дупилумаб
Дупилумаб рекомендован для лечения пациентов со среднетяжёлым и тяжёлым АтД в возрасте от 6 месяцев при недостаточной эффективности топических препаратов или при наличии противопоказаний к их применению[8]. Препарат представляет собой полностью человеческое рекомбинантное моноклональное антитело, блокирующее эффекты ключевых медиаторов Т2-воспаления при АтД — ИЛ-4 и ИЛ-13.
Международные клинические исследования демонстрируют значительное улучшение состояния кожи и уменьшение интенсивности зуда при терапии дупилумабом по сравнению с плацебо. Препарат одобрен для применения в США, Европейском союзе, России и других странах. В России дупилумаб включён в клинические рекомендации и стандарты оказания медицинской помощи пациентам с АтД[9].
Дупилумаб также применяется при бронхиальной астме, узловатой почесухе, хроническом полипозном риносинусите и эозинофильном эзофагите.
Тралокинумаб
Тралокинумаб — моноклональное антитело, нацеленное на ИЛ-13, ключевой медиатор Т2-воспаления при АтД. Препарат не зарегистрирован в России. В Европейском союзе одобрен для лечения пациентов со среднетяжёлым и тяжёлым АтД в возрасте от 12 лет, являющихся кандидатами на системную терапию[8]. Международные клинические исследования показывают значительное улучшение состояния кожи и уменьшение интенсивности зуда при применении тралокинумаба.
Лебрикизумаб
Лебрикизумаб, как и тралокинумаб, блокирует ИЛ-13. Не доступен в России. В Европейском союзе одобрен для применения у пациентов со среднетяжёлым и тяжёлым АтД от 12 лет, являющихся кандидатами на системную терапию[8].
Экспериментальное лечение Немолизумабом
Немолизумаб — гуманизированное моноклональное антитело, специфичное к интерлейкину-31, рассматривается как потенциальное средство лечения АтД. В 2017 году в The New England Journal of Medicine были опубликованы результаты II фазы клинического исследования Немолизумаба для лечения среднетяжёлого и тяжёлого АтД[10].
Иммуносупрессанты
Иммуносупрессанты оказывают противовоспалительное действие путём подавления иммунного ответа[11].
Циклоспорин
Согласно Российским клиническим рекомендациям, терапия циклоспорином может быть назначена взрослым пациентам с тяжёлым течением АтД[6]. Механизм действия циклоспорина основан на подавлении активации и пролиферации Т-клеток, что приводит к уменьшению воспаления[12]. Применение циклоспорина сопровождается значительным снижением выраженности симптомов АтД.
Терапия циклоспорином требует тщательного мониторинга лабораторных показателей до и во время лечения. Необходим контроль биохимических показателей крови, так как препарат может вызывать нежелательные явления: повышение концентрации креатинина и мочевины, гиперлипидемию, гиперурикемию, гиперкалиемию, гипомагниемию, гипергликемию. Возможно дозозависимое обратимое увеличение концентрации билирубина и активности печёночных ферментов. В редких случаях может развиться гепатотоксическое действие с холестазом, желтухой, гепатитом и печёночной недостаточностью.
Контроль общего анализа мочи необходим из-за потенциального токсического воздействия на почки и риска развития инфекционных поражений почек и мочевыводящих путей на фоне иммуносупрессии.
Ингибиторы Янус-киназ[12]
Ингибиторы Янус-киназ (барицитиниб, упадацитиниб, аброцитиниб) относятся к селективным иммунодепрессантам. Их механизм действия основан на воздействии на янус-киназы различных типов — ферменты, обеспечивающие внутриклеточную передачу сигнала от многочисленных рецепторов в рамках сигнального пути JAK-STAT.
Данная группа препаратов применяется при лечении ряда иммуноопосредованных заболеваний, включая ревматоидный артрит. У пациентов с АтД терапия ингибиторами янус-киназ приводит к улучшению состояния кожи и снижению интенсивности зуда.
Ввиду потенциального широкого иммуносупрессивного эффекта, применение препаратов данной группы может иметь ограничения для определённых категорий пациентов. Терапия требует мониторинга лабораторных показателей до и в процессе лечения, а также проведения скрининга на инфекционные заболевания (туберкулёз, гепатит).
Глюкокортикостероиды[12]
Системные глюкокортикостероиды применяются кратковременно при обострениях АтД, так как имеют неблагоприятное соотношение риск/польза при длительном использовании у взрослых и детей. При высоких дозах и продолжительном применении (>0,5 мг/кг/день) возможны серьёзные побочные эффекты: атрофия кожи, увеличение массы тела, нарушения сна, изменения настроения, гипергликемия или диабет, пептические язвы/гастриты, остеопороз и повышенная восприимчивость к инфекциям.
Глюкокортикостероиды — класс стероидных гормонов, связывающихся с глюкокортикоидными рецепторами. Активированный комплекс глюкокортикоидных рецепторов усиливает экспрессию противовоспалительных белков и подавляет экспрессию провоспалительных, обеспечивая широкое противовоспалительное действие.
Несмотря на распространённое применение системных глюкокортикостероидов в клинической практике, исследования их системного применения (перорально или инъекционно) у пациентов с АтД ограничены. Проведённые исследования показывают, что системные глюкокортикостероиды не вызывают длительной ремиссии, и часто наблюдается быстрый рецидив заболевания.
Примечания
- ↑ 1,0 1,1 1,2 Атопический дерматит // Педиатрия : [арх. 30 марта 2017 / Под ред. А.А. Баранова. — ГЭОТАР-Медиа, 2009. — Т. 2.].
- ↑ Атопический дерматит и экзематозные расстройства = Atopic Dermatitis and Eczematous Disorders / Под ред. Дональда Рудикоффа, Стивена Р. Коэна, Ноа Шайнфельда; Пер. с англ. — М.: ГЭОТАР-Медиа, 2017. — 384 с.
- ↑ 3,0 3,1 Ляликов С. А., Гаврилик Л. Л. Клиническая аллергология // Гродно: УО ГрГМУ, 2007. — 200 с. С. 90-91..
- ↑ 4,0 4,1 Diagnostic Features of Atopic Dermatitis.
- ↑ ТАМРАЗОВА, О., & ГЛУХОВА, Е. (2021). Уникальная молекула филаггрин в структуре эпидермиса и её роль в развитии ксероза и патогенеза атопического дерматита. Клиническая дерматология и венерология, 20(6), 102-110.
- ↑ 6,0 6,1 6,2 6,3 6,4 6,5 6,6 Атопический дерматит. Клинические рекомендации МЗ РФ, 2021..
- ↑ 7,0 7,1 7,2 7,3 7,4 7,5 A. Wollenberg, A. Oranje, M. Deleuran, D. Simon, Z. Szalai. ETFAD/EADV Eczema task force 2015 position paper on diagnosis and treatment of atopic dermatitis in adult and paediatric patients (англ.) // Journal of the European Academy of Dermatology and Venereology. — 2016. — Vol. 30, iss. 5. — P. 729–747..
- ↑ 8,0 8,1 8,2 Государственный реестр лекарственных средств..
- ↑ ПРИКАЗ от 25 марта 2022 года N 202н Об утверждении стандарта медицинской помощи детям при атопическом дерматите (диагностика и лечение)..
- ↑ Anti-Interleukin-31 Receptor A Antibody for Atopic Dermatitis Архивная копия от 7 октября 2017 на Wayback Machine The New England Journal of Medicine.
- ↑ Hussain Y, Khan H. Immunosuppressive Drugs. // Encyclopedia of Infection and Immunity. — 2022..
- ↑ Wollenberg A, Kinberger M, Arents B, et al. European guideline (EuroGuiDerm) on atopic eczema: part I - systemic therapy // J Eur Acad Dermatol Venereol. — 2022..